| 1.化学品等及び会社情報 | |||
|---|---|---|---|
| 化学品の名称 | ビフェニル-2-オール(別名2-フェニルフェノール) | ||
| 化学品の英語名称 | Biphenyl-2-ol | ||
| 製品コード | R06-B-062-JNIOSH | ||
| 供給者の会社名 | ○○○○株式会社 | ||
| 住所 | 東京都△△区△△町△丁目△△番地 | ||
| 電話番号 | 03-1234-5678 | ||
| ファクシミリ番号 | 03-1234-5678 | ||
| 電子メールアドレス | 連絡先@検セ.or.jp | ||
| 緊急連絡電話番号 | 03-1234-5678 | ||
| 推奨用途及び使用上の制限 | 防カビ剤,合成繊維用キャリヤー,合成樹脂原料,殺菌剤(失効農薬)(NITE-CHRIPより引用) | ||
| 2.危険有害性の要約 | |||
|---|---|---|---|
| GHS分類 | |||
| 分類実施日 (物化危険性及び健康有害性) | 令和6年度(2024年度)、ガイダンスVer.2.1 (GHS 6版, JIS Z7252:2019) ※一部、平成20年度(2008年度)、ガイダンス(H20.9.5版)(GHS 2版) | ||
| 物理化学的危険性 | - | ||
| 健康に対する有害性 | 皮膚腐食性/刺激性 | 区分1 | |
| 眼に対する重篤な損傷性/眼刺激性 | 区分1 | ||
| 発がん性 | 区分2 | ||
| 分類実施日 (環境有害性) | 令和5年度(2023年度)、ガイダンスVer.2.1 (GHS 6版, JIS Z7252:2019) | ||
| 環境に対する有害性 | 水生環境有害性 短期(急性) | 区分1 | |
| 水生環境有害性 長期(慢性) | 区分1 | ||
| GHSラベル要素 | |||
|---|---|---|---|
| 絵表示 |    | ||
| 注意喚起語 | 危険 | ||
| 危険有害性情報 | 重篤な皮膚の薬傷及び眼の損傷 発がんのおそれの疑い 水生生物に非常に強い毒性 長期継続的影響によって水生生物に非常に強い毒性 | ||
| 注意書き | |||
| 安全対策 | 粉じん/煙/ガス/ミスト/蒸気/スプレーを吸入しないこと。 取扱い後はよく手を洗うこと。 保護手袋/保護衣/保護眼鏡/保護面を着用すること。 使用前に取扱説明書を入手すること。 全ての安全注意を読み理解するまで取り扱わないこと。 環境への放出を避けること。 | ||
| 応急措置 | 飲み込んだ場合:口をすすぐこと。無理に吐かせないこと。 皮膚(又は髪)に付着した場合:直ちに汚染された衣類を全て脱ぐこと。皮膚を水【又はシャワー】で洗うこと。 汚染された衣類を再使用する場合には洗濯をすること。 吸入した場合:空気の新鮮な場所に移し、呼吸しやすい姿勢で休息させること。 直ちに医師に連絡すること。 特別な処置が必要である(このラベルの・・・を見よ)。 注) ”・・・”は、ラベルに解毒剤等中毒時の情報提供を受けるための連絡先などが記載されている場合のものです。ラベル作成時には、”・・・”を適切に置き換えてください。 眼に入った場合:水で数分間注意深く洗うこと。次にコンタクトレンズを着用していて容易に外せる場合は外すこと。その後も洗浄を続けること。 ばく露又はばく露の懸念がある場合:医師の診察/手当てを受けること。 漏出物を回収すること。 | ||
| 保管 | 施錠して保管すること。 | ||
| 廃棄 | 内容物/容器を都道府県知事の許可を受けた専門の廃棄物処理業者に依頼して廃棄すること。 | ||
| 他の危険有害性 | 情報なし | ||
| 3.組成及び成分情報 | |||
|---|---|---|---|
| 化学物質・混合物の区別 | 化学物質 | ||
| 化学名又は一般名 | ビフェニル-2-オール | ||
| 慣用名又は別名 | 2-ヒドロキシビフェニル 2-フェニルフェノール o-フェニルフェノール | ||
| 英語名 | Biphenyl-2-ol | ||
| 濃度又は濃度範囲 | 情報なし | ||
| 分子式 (分子量) | C12H10O (170) | ||
| 化学特性 (示性式又は構造式) | 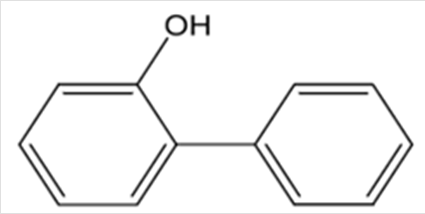 | ||
| CAS番号 | 90-43-7 | ||
| 官報公示整理番号 (化審法) | 4-19 | ||
| 官報公示整理番号 (安衛法) | 7-(3)-140 ( 7-(3)-132 ) | ||
| GHS分類に寄与する成分(不純物及び安定化添加物も含む) | - | ||
| 4.応急措置 | |||
|---|---|---|---|
| 吸入した場合 | 新鮮な空気のある場所に移動し、呼吸しやすい姿勢で安静にさせる。医師に連絡すること。 気分が悪い時や呼吸に関する症状が現れた場合は、医師の診察/手当てを受けること。 意識がないが呼吸がある場合は、横向きに安定した姿勢で寝かせ、低体温症から保護する。 気道/呼吸器疾患の刺激が発生した場合:できるだけ早く、グルココルチコイド吸入スプレーを吸入する。 呼吸困難な場合は酸素吸入をさせる。 以上、GESTIS、ICSC参照。 | ||
| 皮膚に付着した場合 | 直ちに汚染された衣類を全て脱ぐこと。 皮膚刺激または発しん(疹)が生じた場合は、医師の診察/手当てを受けること。皮膚に付着した部分を流水またはシャワーで洗い流したのち、水と石けん(鹸)で丁寧に洗浄する。 ポリエチレングリコール 400 と水を交互に使用してすすぐ。最後に、水と石けん(鹸)で丁寧に洗浄する。 アルコール、ガソリン、その他の溶剤は絶対に使用しない。 以上、GESTIS、ICSC参照。 | ||
| 眼に入った場合 | 水で数分間注意深く洗うこと。次にコンタクトレンズを着用していて容易に外せる場合は外すこと。その後も洗浄を続けること。 眼の刺激が続く場合は医師の診察/手当てを受けること。 以上、GESTIS、ICSC参照。 | ||
| 飲み込んだ場合 | 口をすすぐこと。無理に吐かせないこと。 意識がある場合は、コップ1~2杯の水を飲ませる。 無理に吐かせないこと。 自然嘔吐の場合は、嘔吐物が呼吸器に侵入するのを防ぐため、頭を胸より低くし、うつぶせの姿勢にする。 以上、GESTIS参照。 | ||
| 急性症状及び遅発性症状の最も重要な徴候症状 | 急性: 粘膜、特に眼への刺激。皮膚への刺激、全身への影響に関する十分な情報がない 慢性: 皮膚の変化、さらなる影響に関する十分な情報がない。実験動物では腫瘍が見つけられているが、ヒトへの関連性は不明である。 以上、GESTIS、ICSC参照。 | ||
| 応急措置をする者の保護に必要な注意事項 | 救助者は、状況に応じて適切な眼、皮膚の保護具を着用する | ||
| 医師に対する特別な注意事項 | 情報なし | ||
| 5.火災時の措置 | |||
|---|---|---|---|
| 適切な消火剤 | 水噴霧、乾燥消火剤、アルコール耐性泡消火剤、二酸化炭素 以上、GESTIS、ICSC参照。 | ||
| 使ってはならない消火剤 | 火災が周辺に広がる恐れがあるため、直接の棒状注水を避ける。 | ||
| 特有の危険有害性 | 火災の場合、有害物質(一酸化炭素と二酸化炭素)が放出される可能性がある。 以上、GESTIS参照。 | ||
| 特有の消火方法 | 突然の放出や大量の粉じんの発生に備えて、直ちに避難すること。 可能であれば、容器を危険区域から移動する。 着火(発火)源を遮断する。 流出水が排水システムに入らないようにすること。 以上、GESTIS参照。 | ||
| 消火を行う者の特別な保護具及び予防措置 | 消火作業の際は、適切な自給式の呼吸器用保護具、眼や皮膚を保護する防護服 (耐熱性) を着用する。 以上、GESTIS参照。 | ||
| 6.漏出時の措置 | |||
|---|---|---|---|
| 人体に対する注意事項、保護具及び緊急措置 | 個人用保護具を着用すること(「個人用保護具」の章を参照)。 影響を受ける周囲に警告する。 周囲を換気し、こぼれた場所を洗浄する。 以上、GESTIS参照。 | ||
| 環境に対する注意事項 | 環境への放出を避けること。 可能であれば、閉じた装置を使用すること。 容器とパイプラインにラベルを貼ること。 水への深刻な危険。水、排水、下水、または地中への浸透を防ぐ。 以上、GESTIS参照。 | ||
| 封じ込め及び浄化の方法及び機材 | 漏出物を回収すること。 この物質を環境中に放出してはならない。 こぼれた物質を密閉容器内に収集する。 湿らせてもよい場合は、粉じんを避けるために湿らせてから掃き入れる。 廃棄物を流し台やゴミ箱に入れたり置いたりしない。 収集容器にはラベルを貼ること。 以上、GESTIS、ICSC参照。 | ||
| 二次災害の防止策 | 情報なし | ||
| 7.取扱い及び保管上の注意 | |||
|---|---|---|---|
| 取扱い | |||
| 技術的対策 | 「8. ばく露防止及び保護措置」に記載の措置を行い、必要に応じて保護具を着用する 粉じんを発生させないこと。避けられない粉じんの発生は、定期的に収集すること。 掃除中に粉じんを起こさないこと。 清掃にブロワーを使用しないこと。 以上、GESTIS参照。 | ||
| 安全取扱い注意事項 | 全ての安全注意を読み理解するまで取り扱わないこと。 使用前に取扱説明書を入手すること。 粉じん/煙/ガス/ミスト/蒸気/スプレーを吸入しないこと。 作業場所を清潔に保つこと。 容器を開けたままにしないこと。 補充、移し替え、または開放使用のためには、十分な換気を確保する必要がある。 こぼれないようにすること。 ラベルの付いた容器にのみ注入すること。 粉じんを発生させないこと。 裸火禁止。 粉じんの堆積を防ぐ。 以上、GESTIS、ICSC参照。 | ||
| 接触回避 | 感染性、放射性、爆発性の物質。 ガス。 自然発火性物質。 水と接触した可燃性ガスを放出する物質。 硝酸アンモニウム及び硝酸アンモニウムを含有する製剤 有機過酸化物および自己反応性物質。 危険な化学反応が起こりうる物質と一緒に保管しない。 以上、GESTIS参照。 | ||
| 衛生対策 | 汚染された衣類を再使用する場合には洗濯をすること。 取扱い後はよく手を洗うこと。 眼、皮膚、衣類への接触を避けること。接触した場合は患部を洗浄する。 眼に入った場合は、影響を受けた眼を洗い流す。 以上、GESTIS参照。 | ||
| 保管 | |||
| 安全な保管条件 | 施錠して保管すること。 容器にはラベルを貼付すること。 できるだけ元の容器に保管すること。 密閉すること。 乾燥した場所に保管すること。 強酸化剤、強塩基および食品や飼料から離しておく。 排水溝のない場所で貯蔵する。 以上、GESTIS、ICSC参照。 | ||
| 安全な容器包装材料 | 国連輸送法規で規定されている容器を使用する。 | ||
| 8.ばく露防止及び保護措置 | ||||
|---|---|---|---|---|
| 許容濃度については日本産衛学会の「許容濃度の勧告」及びACGIHの「TLVs and BEIs」について記載しています。 | ||||
| 管理濃度 | - | |||
| 濃度基準値 | ||||
| 八時間濃度基準値 | - | |||
| 短時間濃度基準値 | - | |||
| 許容濃度 | ||||
| 日本産衛学会 (2023年度版) | (吸入性粉じん)2 mg/m3 (総粉じん)8 mg/m3 (第3種粉じん) | |||
| ACGIH (2024年版) | PNOS* TLV: 3 mg/m3 (Respirable particles) PNOS* TLV: 10 mg/m3 (Inhalable particles) * Particles (insoluble or poorly soluble) Not Otherwise Specified | |||
| 設備対策 | 粉じんが発生する作業所においては、必ず密閉された装置、機器または局所換気装置を使用する。 取り扱い場所の近くに洗浄のための設備を設ける。 洗眼設備を設置し、標識を付ける。 作業場の換気を良好に保つこと。 床に排水溝を設置しない。 以上、GESTIS参照。 | |||
| 保護具 | ||||
| 呼吸用保護具 | 緊急時には、呼吸保護具を着用する。 フィルター装置の使用限界を超える濃度、体積18%未満の酸素濃度、または不明な状況では、絶縁装置を使用すること。 以上、GESTIS参照。 | |||
| 手の保護具 | 必要に応じて適切な不浸透性の保護手袋を使用すること。着用する前に締まり具合を確認すること。手袋は取り外す前に十分に洗浄し、換気の良い場所に保管すること。 次の材料は保護手袋に適している(透過時間>= 8時間): ブチルゴム - ブチル(0,5 mm)、フッ素樹脂ゴム - FKM(0,4 mm) 以上、GESTIS参照。 | |||
| 眼の保護具 | 必要に応じて安全眼鏡、保護面、安全ゴーグルなどの眼用保護具を着用する。 以上、GESTIS参照。 | |||
| 皮膚及び身体の保護具 | 必要に応じて保護衣、保護エプロン等を着用する。 | |||
| 9.物理的及び化学的性質 | |||
|---|---|---|---|
| 物理的状態 | |||
| 物理状態 | 固体 | ||
| 色 | 白色~ピンク色 | ||
| 臭い | 甘さのあるフェノール臭 | ||
| 融点/凝固点 | 59 ℃ (HSDB in PubChem(2024)) | ||
| 沸点、初留点及び沸騰範囲 | 286 ℃ (HSDB in PubChem(2024)) | ||
| 可燃性 | 可燃性 (GESTIS(2024)) | ||
| 爆発下限界及び爆発上限界/可燃限界 | 1.4~9.5 vol% (空気中) (ICSC(2013)) | ||
| 引火点 | 124 ℃ (Closed cup) (NFPA (14th, 2010)) 138 ℃ (Closed cup) (HSDB in PubChem(2024)) | ||
| 自然発火点 | 520 ℃ (HSDB in PubChem (2024)) 530 ℃ (NFPA (14th, 2010)) | ||
| 分解温度 | データなし | ||
| pH | データなし | ||
| 動粘性率 | データなし | ||
| 溶解度 | 水:0.2 g/L (ICSC(2013)) 水:620 mg/L (20℃) (MOE初期評価第19巻 (2021)) エタノール、アセトン、ベンゼン、クロロホルム、リグロイン、エチルエーテル、ピリジン、ほとんどの有機溶剤:可溶 (HSDB in PubChem(2024)) | ||
| n-オクタノール/水分配係数 | logKow:3.09 (HSDB in PubChem(2024)) | ||
| 蒸気圧 | 0.002 mmHg (25℃) (HSDB in PubChem(2024)) | ||
| 密度及び/又は相対密度 | 1.213 g/cm3 (25℃) (HSDB in PubChem(2024)) 1.2 (水=1) (相対密度) (NFPA (14th, 2010)) | ||
| 相対ガス密度 | データなし | ||
| 粒子特性 | データなし | ||
| 10.安定性及び反応性 | |||
|---|---|---|---|
| 反応性 | 物質は可燃性である。 以上、GESTIS参照。 | ||
| 化学的安定性 | 通常の取扱い条件下では安定である。 | ||
| 危険有害反応可能性 | 可燃性。 火災時に、刺激性あるいは有毒なフュームやガスを放出する。 空気中で粒子が細かく拡散して、爆発性の混合気体を生じる。 強塩基および強酸化剤と反応する。 加熱により分解する。二酸化炭素、一酸化炭素および刺激性のフュームを生じる。 以上、ICSC参照。 | ||
| 避けるべき条件 | 次の条件が満たされると、粉じん爆発の危険性がある: 非常に細かく分布した形(粉末、粉じん)。空気中で十分な量が渦巻いている。発火源が存在する(炎、火花、静電放電など)。 発火源(火気、加熱、高温、静電気、火花など)に近づけないこと。 以上、GESTIS参照。 | ||
| 混触危険物質 | 酸化剤、還元剤等 | ||
| 危険有害な分解生成物 | 火災の場合、有害物質(一酸化炭素と二酸化炭素)が放出される可能性がある。 以上、GESTIS参照。 | ||
| 11.有害性情報 | |||
|---|---|---|---|
| 急性毒性 | |||
| 経口 | 【分類根拠】 (1)、(2)より区分に該当しない(国連分類基準の区分5)。 【根拠データ】 (1)ラットのLD50:2,733 mg/kg(OECD TG401、GLP)(ECHA RAC Opinion (2022)、EU CLP CLH (2021)、SCCS (2015)、ECHA CHEM (Accessed Aug. 2024)) (2)ラットのLD50:> 2,500~ 2,980 mg/kg(同上) 【参考データ等】 (3)マウスのLD50:1,200 mg/kg(雄)、1,050 mg/kg(雌)(ECHA RAC Opinion (2022)、EU CLP CLH (2021)、MOE初期評価 (2021)、SCCS (2015)) (4)マウスのLD50:3,499 mg/kg(雄)、3,152 mg/kg(雌)(ECHA RAC Opinion (2022)、EU CLP CLH (2021)、SCCS (2015)) | ||
| 経皮 | 【分類根拠】 (1)、(2)より区分に該当しない。 【根拠データ】 (1)ラットのLD50:> 2,000 mg/kg(OECD TG402、GLP)(ECHA RAC Opinion (2022)、 MOE初期評価 (2021)、AICIS IMAP (2015)、SCCS (2015)、ECHA CHEM (Accessed Aug. 2024)) (2)ウサギのLD50:> 5,000 mg/kg(OECD TG402)(同上) | ||
| 吸入: ガス | 【分類根拠】 GHSの定義における固体であり、区分に該当しない。 | ||
| 吸入: 蒸気 | 【分類根拠】 データがなく分類できない。 | ||
| 吸入: 粉じん及びミスト | 【分類根拠】 (1)、(2)からは区分を特定できず分類できない。 【根拠データ】 (1)ラットのLC50(4時間):> 0.036 mg/L(OECD TG403、GLP:達成可能な最高濃度)(RAC Opinion (2022)、AICIS IMAP (2015)、MOE初期評価 (2021)、SCCS (2015)、ECHA CHEM (Accessed August 2024)) (2)ラットのLC50(1時間):> 0.949 mg/L(4時間換算:> 0.238 mg/L)(同上) 【参考データ等】 (3)本物質の最大達成濃度(0.036 mg/L)では死亡例は生じなかった。従って、RAC Opinion (2022) ではno classification(区分に該当しない)を支持している(ECHA RAC Opinion (2022))。 | ||
| 皮膚腐食性及び皮膚刺激性 | 【分類根拠】 (1)より区分1とした。 【根拠データ】 (1)ウサギ(n= 6)を用いた皮膚刺激性試験(OECD TG404、GLP:原体0.5 g、水で湿らせ4時間塗布)において、パッチ除30分以内に4/6例で火傷が72時間後まで認められ、その後痂皮形成が持続し15日目には瘢痕化がみられた(ECHA RAC Opinion (2022)、AICIS IMAP (2015))。本物質は強度又は高度の皮膚刺激性物質と判断された(SCCS (2015)、REACH登録情報 (Accessed August 2024))。 【参考データ等】 (2)ウサギ(n= 6)を用いた皮膚刺激性試験(OECD TG404:4時間塗布)では、パッチ除去72時間後にみられた皮膚刺激性所見は7日後まで持続した(ECHA RAC Opinion (2022)、AICIS IMAP (2015))。本物質は強度の皮膚刺激性物質と判断された(SCCS (2015))。 (3)EUではSkin Irrit. 2に分類されている(CLP分類(Accessed Aug. 2024))が、Skin Corr. 1への変更がECHA RACで合意されている(ECHA RAC Opinion (2022))。 | ||
| 眼に対する重篤な損傷性又は眼刺激性 | 【分類根拠】 (1)~(3)より区分1とした。 【根拠データ】 (1)ウサギ(n= 3)を用いた眼刺激性試験(OECD TG405:原液0.1 mL、非洗浄、8日間観察)において、24/48/72hの個体別平均スコアで角膜混濁(1.67/1.67/2.0)、虹彩炎(1.33/1.33/0.67)、結膜発赤(1.67/2.0/1.33)、結膜浮腫(2.33/2.33/2.0)の眼刺激性がみられた。観察期間終了の8日目には72時間後と比べ、結膜病変(発赤、浮腫)はスコアの低下がみられたが、角膜混濁スコアでは1例で2から3に(他2例はスコア2のまま)、虹彩スコアでは2例で1から2に(他1例はスコア2のまま)、刺激性スコアの増加がみられ、時間とともに影響がより重篤化することが示された。(ECHA RAC Opinion (2022)、AICIS IMAP (2015)、SCCS (2015)、REACH登録情報 (Accessed Aug. 2024)) (2)ウサギを用いた眼刺激試験(OECD TG405:原液0.1 g、7日間観察)において、24/48/72hの個体別平均スコアで角膜混濁(1.33/2.33/2/2.67/3/1.67)、虹彩炎(1/1/2/1/1/1)、結膜発赤(2.67/2.67/3/2.33/2.33/2)、結膜浮腫(3.33/3.33/4/4/4/3)の眼刺激性変化が認められた。試験終了時(7日目)にも4匹の角膜混濁スコア及び6匹の虹彩スコアが72時間後と同じであり、本物質はウサギの眼に7日間の観察期間内に回復性のみられない重篤な眼刺激性を生じた(同上)。 (3)本物質の皮膚刺激性分類は区分1である(2024年度政府GHS分類結果)。 【参考データ等】 (4)EUではEye Irrit. 2に分類されている(CLP分類結果 (Accssed Aug. 2024))が、Eye Dam. 1への変更がECHA RACで合意されている(ECHA RAC Opinion (2022))。 | ||
| 呼吸器感作性 | 【分類根拠】 データがなく分類できない。 | ||
| 皮膚感作性 | 【分類根拠】 (1)、(2)より区分に該当しないとした。 【根拠データ】 (1)モルモット(n= 20)を用いたマキシマイゼーション試験(皮内感作:0.5及び5%、経皮感作:25%、惹起:5%)では、0.5及び5%で惹起後(試験21日目)の陽性率はいずれも0%(0/20)であった(ECHA RAC Opinion (2022)、AICIS IMAP (2015)、ECHA CHEM (Accessed Aug. 2024))。 (2)モルモット(n= 10)を用いた2つのビューラー試験(局所感作:100%、惹起:100%、又は7.5%溶液)では、惹起終了24及び48時間後の陽性率はいずれも0%(0/9又は0/10)であった(同上、SCCS (2015))。 【参考データ等】 (3)男女200人の被験者に本物質(OPP)及び本物質Na塩 (ナトリウム=1,1’‐ビフェニル‐2‐オラート (CAS登録番号 132-27-4)) を塗布した後、皮膚感作の証拠は認められなかった(ECHA RAC Opinion (2022)、AICIS IMAP (2015)、ECHA CHEM (Accessed Aug. 2024))。一方、医療用ハンドクリームや保冷剤に含まれる本物質の使用後にアレルギー性皮膚炎を発症した3例で、本物質パッチテスト陽性が認められたとの報告など陽性の症例報告がある(AICIS IMAP (2015)、ECHA RAC Opinion (2022))。 (4)ドイツ皮膚科情報ネットワーク(IVDK)が収集したパッチテストの試験結果をみると、1990 年から1994年の間に本物質の1%溶液で11,593人のパッチテストが実施されており、そのうち40人(0.3%)で陽性反応がみられたが、64人では刺激反応はみられたものの、感作については曖昧な結果であった(MOE初期評価 (2021))。 | ||
| 生殖細胞変異原性 | 【分類根拠】 (1)、(2)より区分に該当しないとした。 【根拠データ】 (1)In vivoでは、マウスを用いた経口投与による2つの優性致死験で陰性、ラットの骨髄を用いた染色体異常試験(経口投与)、マウス及びラットを用いた染色体異常試験(経口又は混餌投与)で陰性であった。ラットの骨髄を用いた小核試験(経口投与)で陰性、マウスの肝臓と腎臓、ラットの肝臓と胃のDNA損傷の有無を調べたコメット試験で陰性の結果が得られている一方、マウスの肝臓、肺、腎臓、胃、脾臓、脳、膀胱及び骨髄のDNA損傷を調べたコメット試験では肝臓、肺、腎臓、胃及び膀胱で陽性の結果が示された。また、ラットの膀胱上皮のDNA損傷を調べたアルカリ溶出試験試験(混餌投与後に膀胱内に本物質を注入)で陽性の結果が得られた。これらの陽性の結果は毒性が発現する高用量又は非生理的な投与経路でみられる反応で、その他の試験結果は殆ど陰性であった(ECHA RAC Opinion (2022)、MOE初期評価 (2021))。 (2)In vitroでは、細菌を用いた多数の復帰突然変異試験で陰性(一部陽性)、ほ乳類培養細胞を用いた遺伝子突然変異試験(CHO-WBL細胞, hprt遺伝子座)、及び2つのマウスリンフォーマ試験でいずれも陰性、ほ乳類培養細胞を用いた染色体異常試験で陰性(一部陽性)、小核試験で陰性の結果が得られている(ECHA RAC Opinion (2022)、MOE初期評価 (2021))。 | ||
| 発がん性 | 【分類根拠】 ヒトの発がん性に関する情報はない。動物試験では、(1)、(2)より、マウスに肝臓腫瘍、ラットに膀胱腫瘍の発生増加が認められた。しかし(3)と(4)より、これらの試験結果のヒトとの関連性の解釈には未解決の疑問があり、確実に区分1に分類するには不十分な証拠であることから区分2とした。 【根拠データ】 (1)マウスを用いた2年間混餌投与による慢性毒性・発がん性併合試験(OECD TG453)において、雄の中及び高用量(500及び1,000 mg/kg/day)に肝細胞腺腫の有意な発生増加が認められた。また、雄の投与群に肝芽腫の発生があり、量反応関係は明瞭でなかったが、背景データの範囲を超えていた。雌には肝臓腫瘍の増加はなかった(RAC Opinion (2022)、MOE初期評価 (2021))。なお、肝細胞腺腫など肝臓腫瘍の発生増加に関して、カナダの評価では肝臓の腫瘤又は結節の増加と肉眼所見レベルで表現されている(Canada Pesticides (2022))。 (2)ラットを用いた2年間混餌投与による慢性毒性・発がん性併合試験(OECD TG453、GLP)において、雄では膀胱の移行上皮がんが中用量(4,000 ppm:雄/雌:200/248 mg/kg/day)で2/50例、高用量(8,000/10,000 ppm:同402/647 mg/kg/day)で34/50例に認められ、高用量群では膀胱の乳頭腫が6/50例に認められた。一方、雌には膀胱に腫瘍性変化も非腫瘍性変化も認められず、腎臓に非腫瘍性変化(腎結石、過形成、乳頭石灰化等)がみられただけであった(RAC Opinion (2022)、MOE初期評価 (2021)、Canada Pesticides (2022))。 (3)(1)のマウスの肝臓腫瘍については、本物質投与後のマウスの肝臓でPPARα応答性遺伝子(cyp4a10)の発現増加が認められたことから、作用機序はPPARα依存性のげっ歯類の肝臓腫瘍誘発が関与していると考えられた。ヒトに関連する他の作用機序が存在する可能性を除外するためにはより多くの実験的な証拠が必要であるとECHAのRACは述べている(RAC Opinion (2022))。 (4)(2)のラットの膀胱腫瘍の発生の作用機序については、本物質投与後に膀胱内で生じる尿pH、尿中ナトリウム及び尿浸透圧の増加が膀胱上皮に対して持続的な炎症性刺激を及ぼすことが腫瘍誘発の誘因となるとの仮説が提起され、ヒトではこのような作用様式による膀胱腫瘍は生じない。すなわち、膀胱腫瘍はラット特異的な現象と解釈されたが、ECHAのRACは、作用機序には未解明な部分があること、尿pH、尿中ナトリウム及び尿浸透圧の増加はラット特異的な影響であることの説明にはならないことから、ラットの膀胱腫瘍のヒトへの外挿の妥当性は否定されるものではないとの見解を示した(同上)。 【参考データ等】 (5)国内外の評価機関による既存分類では、IARCでグループ3(IARC 73 (1999))、DFGでカテゴリー4(List of MAK and BAT values (2023))に分類されている。ただし、IARCの分類は(1)、(2)を含め標準的な発がん性試験など信頼性の高いデータを含まない評価のための知見が少ない時点での評価である。EU CLP分類ではCarc. 2への分類見込みである(RAC Opinion (2022))。 (6)(1)以外にマウスを用いた試験として、96週間混餌投与(+8週間観察)試験結果があり、本物質投与群では肝細胞がん(雌雄)、肝血管肉腫(雄)の増加傾向がみられ、雄の中用量(10,000 ppm)以上の群で肝細胞がんの有意な増加がみられた。しかしながら、著者は背景データとの比較により、本試験では投与に関連した発がん性影響はないと結論づけた(IARC 73 (1999)、MOE初期評価 (2021))。 (7)(2)以外にラットを用いた試験として、雄ラットを用いた91週間混餌投与試験で膀胱腫瘍(乳頭腫、がん)が認められたとの結果、また本物質のNa塩(OPP-Na)の雌雄ラットを用いた104週間混餌投与による発がん性試験で膀胱腫瘍(主に移行上皮がん)が雌雄に認められたが、雌は雄に比べて膀胱腫瘍の発生数が顕著に少ないとの結果がある(雌は2回繰り返した高用量群(10,000 ppm)で膀胱の総腫瘍数が4及び2であったのに対し、雄の高用量群(20,000 ppm)のそれらは47及び23)。この他、別系統のラットを用いた2年間混餌投与試験では腫瘍性変化を認めなかった(IARC 73 (1999)、MOE初期評価 (2021)、ECHA RAC Opinion (2022))。 | ||
| 生殖毒性 | 【分類根拠】 (1)~(3)より、低体重児あるいは胚胎児死亡がみられたのは、母動物に明瞭な一般毒性(死亡や体重増加抑制)が認められる高用量のみであったことから、区分に該当しないとした。 【根拠データ】 (1)ラットを用いた混餌投与による2つの二世代生殖毒性試験(OECD TG416相当)において、P及びF1雌雄親動物に体重低値、膀胱の組織変化(移行上皮過形成、結石、炎症等)などがみられた最高用量の490 mg/kg/day及び500 mg/kg/dayで、F1及びF2児動物に低体重がみられた以外に一般毒性影響も生殖発生影響も認められなかった(RAC Opinion (2022)、MOE初期評価 (2021)、Canada Pesticides (2022))。なお、いずれの試験でもF1の交配成績として投与群では受胎率の高値がみられたとの結果が記されているが、対照群の受胎率が極端に低い(32%、67%)ためのアーティファクトで、加齢(2回目の交配時:約9ヵ月齢)による可能性が指摘されている(RAC Opinion (2022))。 (2)妊娠ラットを用いた強制経口投与による2つの発生毒性試験(最大1,200又は700 mg/kg/day、妊娠6~15日)において、1つ目の試験では母動物の11/12例が死亡した試験最高用量の1,200 mg/kg/dayは評価不能のため除外し、評価が可能な高用量(600 mg/kg/day)で母動物に顕著な体重増加抑制及び運動失調(投与後数時間持続)、胎児に死亡率増加と体重の低値がみられた。2つ目の試験でも母動物毒性(体重増加抑制)のみられる高用量(700 mg/kg/day)で着床後死亡率の増加が認められた。いずれの試験でも胎児に変異、奇形の増加は認められなかった(RAC Opinion (2022))、MOE初期評価 (2021)、Canada Pesticides (2022)、AICIS IMAP (2015))。 (3)妊娠ウサギを用いた強制経口投与による発生毒性試験(25~250 mg/kg/day、妊娠7~19日)では、母動物に強い毒性(死亡5例、死亡例で胃粘膜潰瘍、消化管出血等、生存例で腎障害(炎症を伴う尿細管変性など))が認められた高用量(250 mg/k/day)群で、発生影響として着床後胚死亡発生率の増加がみられた。着床後胚死亡発生率の増加は明確な母動物毒性がないと考えられる中用量(100 mg/kg/day:投与との関連が不明な死亡例1例以外に記載なし)でもみられた。催奇形影響はみられなかった(RAC Opinion (2022))、MOE初期評価 (2021)、Canada Pesticides (2022))。 【参考データ等】 (4)妊娠マウスを用いた強制経口投与による発生毒性試験(1450~2100 mg/kg/day、妊娠7~15日)では、低用量の1,450 mg/kg/dayから母動物に致死毒性(低用量で19%、中用量で33%、高用量で76%が死亡)がみられ、低用量から早期死亡胚の増加が、外表奇形(口蓋裂、開眼、外脳症)を有する胎児比率の増加が認められている(同上)。ECHA RAC は、マウスで発見されたすべての奇形は、致死率 10% を大幅に超える用量で発生したため、発達毒性の最終的な分類を立証するものではないと指摘している(RAC Opinion (2022))。 | ||
|---|---|---|---|
| 特定標的臓器毒性 (単回ばく露) | 【分類根拠】 (1)~(4)のデータがあるが、経口、経皮経路については区分2範囲内で標的臓器毒性はみられない。吸入経路においても達成可能な濃度において標的臓器毒性はみられていないが、吸入ばく露による気道刺激性について評価を行うための授十分なデータがないことから、分類できないとした。 【根拠データ】 (1)単回経口投与試験において、区分2範囲内でLD50値が求められている試験データはマウスの1試験(LD50:1,200 mg/kg(雄)、1,050 mg/kg(雌))のみである。当該試験で投与後にみられた症状は、自発運動減少、腹臥位(limb position)、よろめき歩行、呼吸数低下であった。剖検所見の記述はない(ECHA RAC Opinion (2022)、MOE初期評価 (2021)、 SCCS (2015))。 (2)ラットを用いた単回経口投与試験では、雄ラットを用いた試験(LD50:2,980 mg/kg)で麻酔、全身状態不良、腹臥位、側臥位がみられたとの報告、雌雄ラットを用いた試験(LD50:2,733 mg/kg)では2500 mg/kg以上で投与後に流涙、唾液分泌、紅涙、呼吸困難、活動性の低下、側臥位、会陰部の糞尿による汚れがみられ、死亡例の剖検では消化管内の溶血、会陰部の汚れ、前胃部分の漿膜と肝臓の間のフィブリン性癒着が認められたとの報告がある(ECHA RAC Opinion (2022)、SCCS (2015)、ECHA CHEM (Accessed August 2024))。 (3)ラットを用いた単回経皮投与試験(OECD TG402、LD50:> 2,000 mg/kg)では局所の刺激症状(発赤、痂皮)に限られる。剖検で投与に関連した異常は認められなかった(ECHA RAC Opinion (2022)、MOE初期評価 (2021)、AICIS IMAP (2015)、SCCS (2015)、ECHA CHEM (Accessed August 2024))。 (4)ラットを用いた単回吸入ばく露試験(OECD TG403、LC50(4時間)> 0.036 mg/L)では、ばく露後に雌雄の数例で全身の汚れ、雌1例で会陰部の汚れがみられたが、翌日には正常に復していた。剖検で異常は認められなかった(同上)。 | |||
|---|---|---|---|---|
| 特定標的臓器毒性 (反復ばく露) | 【分類根拠】 (1)~(5)より有害影響は経口経路では区分2超の用量で生じ、区分に該当しないと考えられる。ただし、経皮経路では短期間の試験に限られ、吸入経路の試験データはない。経口以外のばく露経路では分類に十分な情報がないため、分類できない。 【根拠データ】 (1)ラットを用いた13週間混餌投与試験では、区分2超の0.313%(雄/雌:391/411 mg/kg/day)で肝臓の絶対・相対重量の増加、1.25%(同1,669/1,650 mg/kg/day)以上で膀胱粘膜上皮の異常増殖、腺血尿、腎臓の炎症等がみられた(ECHA RAC (2022)、MOE初期評価 (2021))。 (2)ラットを用いた2年間混餌投与による慢性毒性/発がん性併合試験では、4,000 ppm(雄/雌:200/248 mg/kg/day)以上の雄で膀胱上皮の過形成、8,000 /10,000 ppm(同402/647 mg/kg/day)では雄には主に膀胱に、雌には主に腎臓に結石を含む非腫瘍性変化がみられる(ECHA RAC (2022)、MOE初期評価 (2021)、Canada Pesticides (2022)、ECHA CHEM (Accessed Aug. 2024))。 (3)マウスを用いた2年間混餌投与による発がん性試験では、250 mg/kg/day以上で主に肝臓に変性細胞巣の増加、脂肪性変化を伴う肝細胞空胞化、肝細胞壊死等がみられる(同上)。 (4)イヌを用いた1ヵ月強制経口投与試験(5日/週)では、200 mg/kg/day以上で嘔吐を生じ、高用量群は6日目以降400 mg/kg/dayから300 mg/kg/dayに用量を下げた。本試験では区分2範囲の100及び400/300 mg/kg/day(90日換算:約22及び72 mg/kg/day)で、主に雄で赤血球数、ヘマトクリット、ヘモグロビンの減少傾向、雌雄で血小板数の減少傾向がみられたが、統計学的に有意な変化ではなかった(ECHA RAC Opinion (2022))。 (5)イヌを用いた1年間強制経口投与による慢性毒性試験では、100及び300 mg/kg/dayで全例に投与期間を通して嘔吐がみられた以外に、投与過誤と推定された2例の死亡がみられただけであった(ECHA RAC Opinion (2022)、ECHA CHEM(Accessed Aug. 2024))。 【参考データ等】 (6)ラットを用いた21日間経皮投与試験、またマウスを用いた4週間経皮投与試験では適用部位に刺激性変化(ラット:過角化及びアカントーシス、マウス:潰瘍性病変)がみられたが、全身毒性影響は認められなかった(ECHA RAC Opinion (2022)、AICIS IMAP (2015)、ECHA CHEM (Accessed Aug. 2024))。 | |||
| 誤えん有害性* | 【分類根拠】 データがなく分類できない。 | |||
| * JIS Z7252の改訂により吸引性呼吸器有害性から項目名が変更となった。 | ||||
| 12.環境影響情報 | |||
|---|---|---|---|
| 生態毒性 | |||
| 水生環境有害性 短期(急性) | 魚類(ニジマス)96時間LC50 (OECD TG203類似、GLP) =4.0 mg/L(EU CLP CLH (2021)、EPA Pesticides RED (2006))、Na塩による甲殻類(アミ科(Americamysis bahia))48時間EC50 (OPPTS 850.1035、GLP) =0.32 mg/L(環境省リスク評価第19巻 (2021)、EU CLP CLH (2021))、藻類(ラフィドセリス属)72時間ErC50 =3.57 mg/L(環境省リスク評価第19巻 (2021)、EU CLP CLH (2021))。以上の結果から、甲殻類より区分1に該当するとした。 | ||
| 水生環境有害性 長期(慢性) | 3種の栄養段階全てに対して慢性水性毒性データが得られている。急速分解性であり(14日間酸素消費量(化審法ガイドライン、GLP):65%、86%、47%(METI既存点検結果 (1980));数種のガイドライン試験に10-day windowが > 60%の試験がみられる(EU CLP CLH (2021)))、魚類(ファットヘッドミノー)の21日間NOEC (OECD TG234, 229, 230類似, GLP)=0.036 mg/L(EU CLP CLH (2021))、甲殻類(オオミジンコ)の21日間NOEC (OECD TG211, GLP)=0.009 mg/L(環境省リスク評価第19巻 (2021))及び0.006 mg/L(EU CLP CLH (2021))、藻類(ラフィドセリス属)の72時間NOErC(OECD TG201、GLP)=0.468 mg/L(環境省リスク評価第19巻 (2021)、EU CLP CLH (2021))のため、甲殻類より区分1に該当するとした。 新たな情報を入手し、採用したので、旧分類から分類結果を変更した。 | ||
| 残留性・分解性 | 化審法分解度試験:良分解性(化学物質安全性点検結果等(分解性・蓄積性)) | ||
| 生態蓄積性 | - | ||
| 土壌中の移動性 | - | ||
| オゾン層への有害性 | 当該物質はモントリオール議定書の附属書A~C及びEに列記されていない。 | ||
| 13.廃棄上の注意 | |||
|---|---|---|---|
| 化学品(残余廃棄物)、当該化学品が付着している汚染容器及び包装の安全で、かつ、環境上望ましい廃棄、又はリサイクルに関する情報 | 廃棄においては、関連法規ならびに地方自治体の基準に従うこと。 都道府県知事などの許可を受けた産業廃棄物処理業者、もしくは地方公共団体がその処理を行っている場合にはそこに委託して処理する。 廃棄物の処理を委託する場合、処理業者等に危険性、有害性を十分告知の上処理を委託する。 容器は洗浄してリサイクルするか、関連法規制並びに地方自治体の基準に従って適切な処分を行う。 空容器を廃棄する場合は、内容物を完全に除去すること。 | ||
| 14.輸送上の注意 | ||||
|---|---|---|---|---|
| 本物質のGHS分類結果に基づく国際規制の分類等は、以下の通りと推定されるが、該否は製品によって異なる場合がある。輸送危険物の分類は、容器等級を含め、荷送人が責任をもって判断することとされているため、輸送の際には、個々の貨物について、製品の状態、形状等も考慮し、輸送モード (航空、船舶) を規制する法規に沿って事業者が判断する必要がある。 | ||||
| 国際規制 | ||||
| 国連番号 | 1759 | |||
| 品名(国連輸送名) | その他の腐食性固体、他に品名が明示されていないもの | |||
| 国連分類 | 8 | |||
| 副次危険 | - | |||
| 容器等級 | III | |||
| 海洋汚染物質 | 該当する | |||
| MARPOL73/78附属書Ⅱ及びIBCコードによるばら積み輸送される液体物質 | 該当しない | |||
| 国内規制 | ||||
| 海上規制情報 | 船舶安全法の規定に従う。 | |||
| 航空規制情報 | 航空法の規定に従う。 | |||
| 陸上規制情報 | 該当しない | |||
| 特別な安全上の対策 | 該当しない | |||
| その他 (一般的) 注意 | 輸送に際しては、直射日光を避け、容器の破損、腐食、漏れのないように積み込み、荷崩れの防止を確実に行う。 重量物を上積みしない。 | |||
| 緊急時応急措置指針番号* | 153 | |||
| * 北米緊急時応急措置指針に基づく。米国運輸省が中心となって発行した「2024 Emengency Response Guidebook」に掲載されている。 | ||||
| 15.適用法令 | ||||
|---|---|---|---|---|
| 法規制情報は作成年月日時点に基づいて記載されております。事業場において記載するに当たっては、最新情報を確認してください。 | ||||
| 労働安全衛生法 | 名称等を表示すべき危険物及び有害物(法第57条第1項、施行令第18条、労働安全衛生規則別表第2)【1684 2-フェニルフェノール】(令和8年4月1日以降) 名称等を通知すべき危険物及び有害物(法第57条の2、施行令第18条の2、労働安全衛生規則別表第2)【1684 2-フェニルフェノール】(令和8年4月1日以降) 危険性又は有害性等を調査すべき物(法第57条の3)(令和8年4月1日以降) | |||
| 労働基準法 | 疾病化学物質(法第75条第2項、施行規則第35条別表第1の2第4号1) 【フェニルフェノール】 | |||
| 化学物質排出把握管理促進法 (PRTR法) | 第一種指定化学物質(法第2条第2項、施行令第1条別表第1) 【388 2フェニルフェノール】 | |||
| 毒物及び劇物取締法 | - | |||
| 船舶安全法 | 腐食性物質(危規則第3条危険物告示別表第1) | |||
| 航空法 | 腐食性物質(施行規則第194条危険物告示別表第1) | |||
| 港則法 | その他の危険物・腐食性物質(法第20条第2項、規則第12条、危険物の種類を定める告示別表) | |||
| 大気汚染防止法 | 有害大気汚染物質に該当する可能性がある物質(中央環境審議会第9次答申) 【181 2-フェニルフェノール】 | |||
| 水質汚濁防止法 | 指定物質(法第2条第4項、施行令第3条の3) 【55 フェノール類及びその塩類】 | |||
| 16.その他の情報 | ||||
|---|---|---|---|---|
| 参考文献 | ||||
| 9項、11項については各データ毎に記載。その他の各項については以下を参照。 ・NITE化学物質総合情報提供システム(NITE-CHRIP) ・International Chemical Safety Cards (ICSC) ・Hazardous Substances Data Bank (HSDB) ・GESTIS Substance database (GESTIS) ・2024 Emengency Response Guidebook ・一般社団法人日本化学工業協会 編「GHS対応ガイドライン ラベル及び表示・安全デ-タシ-ト作成指針」 ・厚生労働省「皮膚障害等防止用保護具の選定マニュアル第1版」 | ||||