| 侾丏壔妛昳摍媦傃夛幮忣曬 | |||
|---|---|---|---|
| 壔妛昳偺柤徧 | (俆亅僋儘儘亅俀亅儊僩僉僔亅係亅儊僠儖僺儕僕儞亅俁亅僀儖)(俀丆俁丆係亅僩儕儊僩僉僔亅俇亅儊僠儖僼僃僯儖)儊僞僲儞乮暿柤僺儕僆僼僃僲儞乯 | ||
| 壔妛昳偺塸岅柤徧 | (5-chloro-2-methoxy-4-methylpyridin-3-yl)-(2,3,4-trimethoxy-6-methylphenyl)methanone | ||
| 惢昳僐乕僪 | R06-S75-JNIOSH | ||
| 嫙媼幰偺夛幮柤 | 仜仜仜仜姅幃夛幮 | ||
| 廧強 | 搶嫗搒仮仮嬫仮仮挰仮挌栚仮仮斣抧 | ||
| 揹榖斣崋 | 03-1234-5678 | ||
| 僼傽僋僔儈儕斣崋 | 03-1234-5678 | ||
| 揹巕儊乕儖傾僪儗僗 | 楢棈愭仐専僙.or.jp | ||
| 嬞媫楢棈揹榖斣崋 | 03-1234-5678 | ||
| 悇彠梡搑媦傃巊梡忋偺惂尷 | 忣曬側偟 | ||
| 俀丏婋尟桳奞惈偺梫栺 | |||
|---|---|---|---|
| GHS暘椶 | |||
| 暘椶幚巤擔 (暔壔婋尟惈媦傃寬峃桳奞惈) | 椷榓2擭搙(2020擭搙)丄僈僀僟儞僗Ver.2.0 (GHS 6斉, JIS Z7252:2019) | ||
| 暔棟壔妛揑婋尟惈 | - | ||
| 寬峃偵懳偡傞桳奞惈 | 旂晢姶嶌惈 | 嬫暘1B | |
| 暘椶幚巤擔 (娐嫬桳奞惈) | 椷榓3擭搙(2021擭搙)丄僈僀僟儞僗Ver.2.0 (GHS 6斉, JIS Z7252:2019) | ||
| 娐嫬偵懳偡傞桳奞惈 | 悈惗娐嫬桳奞惈丂抁婜乮媫惈乯 | 嬫暘2 | |
| 悈惗娐嫬桳奞惈丂挿婜乮枬惈乯 | 嬫暘1 | ||
| 俧俫俽儔儀儖梫慺 | |||
|---|---|---|---|
| 奊昞帵 |   | ||
| 拲堄姭婲岅 | 寈崘 | ||
| 婋尟桳奞惈忣曬 | 傾儗儖僊乕惈旂晢斀墳傪婲偙偡偍偦傟 悈惗惗暔偵撆惈 挿婜宲懕揑塭嬁偵傛偭偰悈惗惗暔偵旕忢偵嫮偄撆惈 | ||
| 拲堄彂偒 | |||
| 丂埨慡懳嶔 | 暡偠傫乛墝乛僈僗乛儈僗僩乛忲婥乛僗僾儗乕偺媧擖傪旔偗傞偙偲丅 墭愼偝傟偨嶌嬈堖偼嶌嬈応偐傜弌偝側偄偙偲丅 曐岇庤戃乛曐岇堖乛曐岇娽嬀乛曐岇柺傪拝梡偡傞偙偲丅 娐嫬傊偺曻弌傪旔偗傞偙偲丅 | ||
| 丂墳媫慬抲 | 旂晢偵晅拝偟偨応崌丗懡検偺悈乛愇偗傫(尣)偱愻偆偙偲丅 旂晢巋寖枖偼敪偟傫(怾)偑惗偠偨応崌丗堛巘偺恌嶡乛庤摉偰傪庴偗傞偙偲丅 摿暿側張抲偑昁梫偱偁傞(偙偺儔儀儖偺丒丒丒傪尒傛)丅 拲乯丂乭丒丒丒乭偼丄儔儀儖偵夝撆嵻摍拞撆帪偺忣曬採嫙傪庴偗傞偨傔偺楢棈愭側偳偑婰嵹偝傟偰偄傞応崌偺傕偺偱偡丅儔儀儖嶌惉帪偵偼丄乭丒丒丒乭傪揔愗偵抲偒姺偊偰偔偩偝偄丅 墭愼偝傟偨堖椶傪扙偓丄嵞巊梡偡傞応崌偵偼愻戵傪偡傞偙偲丅 楻弌暔傪夞廂偡傞偙偲丅 | ||
| 丂攑婞 | 撪梕暔乛梕婍傪搒摴晎導抦帠偺嫋壜傪庴偗偨愱栧偺攑婞暔張棟嬈幰偵埶棅偟偰攑婞偡傞偙偲丅 | ||
| 懠偺婋尟桳奞惈 | 忣曬側偟 | ||
| 俁丏慻惉媦傃惉暘忣曬 | |||
|---|---|---|---|
| 壔妛暔幙丒崿崌暔偺嬫暿 | 壔妛暔幙 | ||
| 壔妛柤枖偼堦斒柤 | (俆亅僋儘儘亅俀亅儊僩僉僔亅係亅儊僠儖僺儕僕儞亅俁亅僀儖)(俀丆俁丆係亅僩儕儊僩僉僔亅俇亅儊僠儖僼僃僯儖)儊僞僲儞 | ||
| 姷梡柤枖偼暿柤 | 僺儕僆僼僃僲儞 | ||
| 塸岅柤 | (5-chloro-2-methoxy-4-methylpyridin-3-yl)-(2,3,4-trimethoxy-6-methylphenyl)methanone | ||
| 擹搙枖偼擹搙斖埻 | 忣曬側偟 | ||
| 暘巕幃 (暘巕検) | C18H20ClNO5 (365.8) | ||
| 壔妛摿惈 (帵惈幃枖偼峔憿幃) | 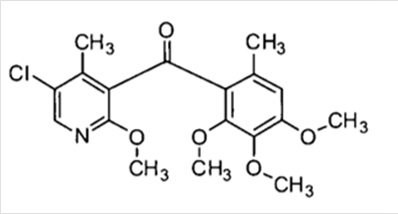 | ||
| CAS斣崋 | 688046-61-9 | ||
| 姱曬岞帵惍棟斣崋 (壔怰朄) | - | ||
| 姱曬岞帵惍棟斣崋 (埨塹朄) | 8-(1)-3380 | ||
| GHS暘椶偵婑梌偡傞惉暘乮晄弮暔媦傃埨掕壔揧壛暔傕娷傓乯 | - | ||
| 係丏墳媫慬抲 | |||
|---|---|---|---|
| 媧擖偟偨応崌 | 嬻婥偺怴慛側応強偵堏偟丄屇媧偟傗偡偄巔惃偱媥懅偝偣傞偙偲丅 徢忬偑懕偔応崌偵偼丄堛巘偵楢棈偡傞偙偲丅 | ||
| 旂晢偵晅拝偟偨応崌 | 旂晢巋寖枖偼敪偟傫(怾)偑惗偠偨応崌丗堛巘偺恌嶡乛庤摉偰傪庴偗傞偙偲丅 懡検偺悈乛愇偗傫(尣)偱愻偆偙偲丅 徢忬偑懕偔応崌偵偼丄堛巘偵楢棈偡傞偙偲丅 | ||
| 娽偵擖偭偨応崌 | 悈偱15乣20暘娫拲堄怺偔愻偆偙偲丅師偵丄僐儞僞僋僩儗儞僘傪拝梡偟偰偄偰梕堈偵奜偣傞応崌偼奜偡偙偲丅偦偺屻傕愻忩傪懕偗傞偙偲丅徢忬偑懕偔応崌偵偼丄堛巘偵楢棈偡傞偙偲丅 | ||
| 堸傒崬傫偩応崌 | 悈偱岥傪偡偡偓丄捈偪偵堛巘偺恌抐傪庴偗傞偙偲 | ||
| 媫惈徢忬媦傃抶敪惈徢忬偺嵟傕廳梫側挜岓徢忬 | 忣曬側偟 | ||
| 墳媫慬抲傪偡傞幰偺曐岇偵昁梫側拲堄帠崁 | 媬彆幰偼丄忬嫷偵墳偠偰揔愗側娽丄旂晢偺曐岇嬶傪拝梡偡傞丅 | ||
| 堛巘偵懳偡傞摿暿側拲堄帠崁 | 忣曬側偟 | ||
| 俆丏壩嵭帪偺慬抲 | |||
|---|---|---|---|
| 揔愗側徚壩嵻 | 悈暚柖丄暡枛徚壩嵻丄朅徚壩嵻丄擇巁壔扽慺傪巊梡偡傞丅 | ||
| 巊偭偰偼側傜側偄徚壩嵻 | 壩嵭偑廃曈偵峀偑傞嫲傟偑偁傞偨傔丄捈愙偺朹忬拲悈傪旔偗傞丅 | ||
| 摿桳偺婋尟桳奞惈 | 堦斒揑側拲堄偲偟偰丄暡枛忬暔幙偺応崌偼丄偁傞忦審壓偱偼暡偠傫敋敪傪婲偙偡壜擻惈偑偁傞丅 | ||
| 摿桳偺徚壩曽朄 | 壩尦傊偺擱從尮傪抐偪丄徚壩嵻傪巊梡偟偰徚壩偡傞丅 墑從偺嫲傟偺側偄傛偆悈僗僾儗乕偱廃埻偺僞儞僋丄寶暔摍偺椻媝傪偡傞丅 徚壩妶摦偼晽忋偐傜峴偆丅 壩嵭応強偺廃曈偵偼娭學幰埲奜偺棫偪擖傝傪婯惂偡傞丅 婋尟偱側偗傟偽壩嵭嬫堟偐傜梕婍傪堏摦偡傞丅 | ||
| 徚壩傪峴偆幰偺摿暿側曐岇嬶媦傃梊杊慬抲 | 徚壩嶌嬈偺嵺偼丄揔愗側帺媼幃偺屇媧婍梡曐岇嬶丄娽傗旂晢傪曐岇偡傞杊岇暈(懴擬惈)傪拝梡偡傞丅 | ||
| 俇丏楻弌帪偺慬抲 | |||
|---|---|---|---|
| 恖懱偵懳偡傞拲堄帠崁丄曐岇嬶媦傃嬞媫慬抲 | 曐岇庤戃乛曐岇堖乛曐岇娽嬀乛曐岇柺傪拝梡偡傞偙偲丅 娭學幰埲奜偺棫偪擖傝傪嬛巭偡傞丅 嶌嬈幰偼揔愗側曐岇嬶(乽8.偽偔業杊巭媦傃曐岇慬抲乿偺崁傪嶲徠)傪拝梡偟丄娽丄旂晢傊偺愙怗傗媧擖傪旔偗傞丅 | ||
| 娐嫬偵懳偡傞拲堄帠崁 | 娐嫬傊偺曻弌傪旔偗傞偙偲丅 廃曈娐嫬偵塭嬁偑偁傞壜擻惈偑偁傞偨傔丄惢昳偺娐嫬拞傊偺棳弌傪旔偗傞丅 | ||
| 晻偠崬傔媦傃忩壔偺曽朄媦傃婡嵽 | 楻弌暔傪夞廂偡傞偙偲丅 墭愼偝傟偨嶌嬈堖偼嶌嬈応偐傜弌偝側偄偙偲丅 旘嶶偟偨暔傪憒偒廤傔傞偐丄恀嬻憒彍婡偱媧堷偡傞摍偱偒傞偩偗旘嶶敪偠傫偟側偄傛偆偵偟偰丄嬻梕婍摍偵夞廂偡傞丅 | ||
| 擇師嵭奞偺杊巭嶔 | 忣曬側偟 | ||
| 俈丏庢埖偄媦傃曐娗忋偺拲堄 | |||
|---|---|---|---|
| 庢埖偄 | |||
| 媄弍揑懳嶔 | 乽8.偽偔業杊巭媦傃曐岇慬抲乿偵婰嵹偺慬抲傪峴偄丄昁梫偵墳偠偰曐岇嬶傪拝梡偡傞丅 | ||
| 埨慡庢埖偄拲堄帠崁 | 暡偠傫乛墝乛僈僗乛儈僗僩乛忲婥乛僗僾儗乕偺媧擖傪旔偗傞偙偲丅 暡偠傫傪敪惗偝偣側偄傛偆偵偡傞丅 | ||
| 愙怗夞旔 | 乽10. 埨慡惈媦傃斀墳惈乿傪嶲徠丅 | ||
| 塹惗懳嶔 | 墭愼偝傟偨堖椶傪扙偓丄嵞巊梡偡傞応崌偵偼愻戵傪偡傞偙偲丅 庢埖偄屻偼傛偔庤傪愻偆偙偲丅 偙偺惢昳傪巊梡偡傞帪偵丄堸怘枖偼媔墝偟側偄偙偲丅 | ||
| 曐娗 | |||
| 埨慡側曐娗忦審 | 曐娗応強偵偼婋尟丒桳奞暔傪挋憼偟丄枖偼庢傝埖偆偨傔偵昁梫側徠柧媦傃姺婥偺愝旛傪愝偗傞丅 | ||
| 埨慡側梕婍曪憰嵽椏 | 崙楢桝憲朄婯偱婯掕偝傟偰偄傞梕婍傪巊梡偡傞丅 | ||
| 俉丏偽偔業杊巭媦傃曐岇慬抲 | ||||
|---|---|---|---|---|
| 嫋梕擹搙偵偮偄偰偼擔杮嶻塹妛夛偺乽嫋梕擹搙偺姪崘乿媦傃ACGIH偺乽TLVs and BEIs乿偵偮偄偰婰嵹偟偰偄傑偡丅 | ||||
| 娗棟擹搙 | - | |||
| 擹搙婎弨抣 | ||||
| 敧帪娫擹搙婎弨抣 | - | |||
| 抁帪娫擹搙婎弨抣 | - | |||
| 嫋梕擹搙 | ||||
| 擔杮嶻塹妛夛 (2024擭搙斉) | (媧擖惈暡偠傫)2 mg/m3 (憤暡偠傫)8 mg/m3 (戞3庬暡偠傫) | |||
| ACGIH (2024擭斉) | PNOS* TLV: 3 mg/m3 (Respirable particles) PNOS* TLV: 10 mg/m3 (Inhalable particles) * Particles (insoluble or poorly soluble) Not Otherwise Specified | |||
| 愝旛懳嶔 | 暡偠傫偑敪惗偡傞嶌嬈強偵偍偄偰偼丄昁偢枾暵偝傟偨憰抲丄婡婍傑偨偼嬊強姺婥憰抲傪巊梡偡傞丅 | |||
| 曐岇嬶 | ||||
| 屇媧梡曐岇嬶 | 暡偠傫偑敪惗偡傞応崌丄昁梫偵墳偠偰曐岇儅僗僋傗屇媧梡曐岇嬶傪拝梡偡傞丅 | |||
| 庤偺曐岇嬶 | 庤偵愙怗偡傞嫲傟偑偁傞応崌丄晄怹摟惈偺曐岇庤戃傪拝梡偡傞丅 岤惗楯摥徣乽旂晢忈奞摍杊巭梡曐岇嬶偺慖掕儅僯儏傾儖乿嶲徠偺偙偲丅 | |||
| 娽偺曐岇嬶 | 娽偵擖傞嫲傟偑偁傞応崌丄曐岇娽嬀傗僑乕僌儖傪拝梡偡傞丅 | |||
| 旂晢媦傃恎懱偺曐岇嬶 | 昁梫偵墳偠偰晄怹摟惈偺曐岇堖丄曐岇僄僾儘儞摍傪拝梡偡傞丅 | |||
| 俋丏暔棟揑媦傃壔妛揑惈幙 | |||
|---|---|---|---|
| 暔棟揑忬懺 | |||
| 暔棟忬懺 | 屌懱 | ||
| 怓 | 敀怓 | ||
| 廘偄 | 僨乕僞側偟 | ||
| 梈揰乛嬅屌揰 | 93乣95 亷(CLH report (2018)) | ||
| 暒揰丄弶棷揰媦傃暒摣斖埻 | 100亷傪挻偊傞偲暘夝偡傞(CLH report (2018)) | ||
| 壜擱惈 | 堷壩惈偼崅偔側偄(CLH report (2018)) | ||
| 敋敪壓尷奅媦傃敋敪忋尷奅乛壜擱尷奅 | 僨乕僞側偟 | ||
| 堷壩揰 | 僨乕僞側偟 | ||
| 帺慠敪壩揰 | 378 亷(CLH report (2018)) | ||
| 暘夝壏搙 | >100 亷(CLH report (2018)) | ||
| pH | 僨乕僞側偟 | ||
| 摦擲惈棪 | 僨乕僞側偟 | ||
| 梟夝搙 | 悈丗1.56 mg/L(20亷丄pH 6.6) (CLH report (2018)) | ||
| n-僆僋僞僲乕儖乛悈暘攝學悢 | log Pow丗3.2(20亷丄pH 7.2乣7.5) (CLH report (2018)) | ||
| 忲婥埑 | 1.9亊10-6 Pa(25亷)(CLH report (2018)) | ||
| 枾搙媦傃乛枖偼憡懳枾搙 | 1.33(CLH report (2018)) | ||
| 憡懳僈僗枾搙 | 僨乕僞側偟 | ||
| 棻巕摿惈 | 僨乕僞側偟 | ||
| 侾侽丏埨掕惈媦傃斀墳惈 | |||
|---|---|---|---|
| 斀墳惈 | 捠忢偺庢埖偄忦審壓偱偼埨掕偱偁傞丅 | ||
| 壔妛揑埨掕惈 | 捠忢偺庢埖偄忦審壓偱偼埨掕偱偁傞丅 | ||
| 婋尟桳奞斀墳壜擻惈 | 捠忢偺庢埖偄忦審壓偱偼婋尟桳奞斀墳傪婲偙偝側偄丅 | ||
| 旔偗傞傋偒忦審 | 捈幩擔岝傪旔偗丄椻埫強偵曐娗偡傞丅 | ||
| 崿怗婋尟暔幙 | 巁壔嵻丄娨尦嵻摍 | ||
| 婋尟桳奞側暘夝惗惉暔 | 壩嵭摍偺応崌偼丄撆惈偺嫮偄暘夝惗惉暔偑敪惗偡傞壜擻惈偑偁傞丅 | ||
| 侾侾丏桳奞惈忣曬 | |||
|---|---|---|---|
| 媫惈撆惈 | |||
| 宱岥 | (侾)傛傝丄嬫暘偵奩摉偟側偄丅 亂崻嫆僨乕僞亃 (侾)儔僢僩(帗)偺LD50丗> 2,000 mg/kg(OECD TG 423丄GLP)(怘埨埾 擾栻昡壙彂 (2018)丄CLH Report (2018)丄ECHA RAC Opinion (2019)) | ||
| 宱旂 | (侾)丄(俀)傛傝丄嬫暘偵奩摉偟側偄丅 亂崻嫆僨乕僞亃 (侾)儔僢僩(梇)偺LD50丗> 2,000 mg/kg(OECD TG 402丄GLP)(怘埨埾 擾栻昡壙彂 (2018)丄CLH Report (2018)丄ECHA RAC Opinion (2019)) (俀)儔僢僩(帗)偺LD50丗> 2,000 mg/kg(OECD TG 402丄GLP)(怘埨埾 擾栻昡壙彂 (2018)丄CLH Report (2018)丄ECHA RAC Opinion (2019)) | ||
| 媧擖: 僈僗 | GHS偺掕媊偵偍偗傞屌懱偱偁傝丄嬫暘偵奩摉偟側偄丅 | ||
| 媧擖: 忲婥 | 僨乕僞晄懌偺偨傔暘椶偱偒側偄丅 | ||
| 媧擖: 暡偠傫媦傃儈僗僩 | (侾)丄(俀)傛傝丄嬫暘偵奩摉偟側偄丅 亂崻嫆僨乕僞亃 (侾)儔僢僩(梇)偺LD50(4帪娫)丗> 5.18 mg/L(OECD TG 403丄GLP)(怘埨埾 擾栻昡壙彂 (2018)丄CLH Report (2018)丄ECHA RAC Opinion (2019)) (俀)儔僢僩(帗)偺LD50(4帪娫)丗> 5.18 mg/L(OECD TG 403丄GLP)(怘埨埾 擾栻昡壙彂 (2018)丄CLH Report (2018)丄ECHA RAC Opinion (2019)) | ||
| 旂晢晠怘惈媦傃旂晢巋寖惈 | (侾)傛傝丄嬫暘偵奩摉偟側偄丅 亂崻嫆僨乕僞亃 (侾)僂僒僊(n=3)傪梡偄偨旂晢巋寖惈帋尡(OECD TG 404丄GLP丄敿暵嵡丄4帪娫揔梡丄72帪娫娤嶡)偵偍偄偰丄慡椺偱旂晢巋寖惈斀墳偼傒傜傟側偐偭偨(峠斄丒醥旂僗僐傾丗0/0/0丄晜庮僗僐傾丗0/0/0)偲偺曬崘偑偁傞(怘埨埾 擾栻昡壙彂 (2018)丄ECHA RAC Opinion (2019)丄CLH Report (2018)丄JMPR (2019)丄擾栻彺榐 (2015))丅 | ||
| 娽偵懳偡傞廳撃側懝彎惈枖偼娽巋寖惈 | (侾)傛傝丄嬫暘偵奩摉偟側偄丅 亂崻嫆僨乕僞亃 (侾)僂僒僊(n=3)傪梡偄偨娽巋寖惈帋尡(OECD TG 405丄GLP丄72帪娫娤嶡)偵偍偄偰丄24帪娫屻偵2椺偱寉旝側寢枌敪愒偑傒傜傟偨偑丄48帪娫屻偵偼徚幐偟偨(妏枌崿戺僗僐傾丗0/0/0丄擑嵤墛僗僐傾丗0/0/0丄寢枌敪愒僗僐傾丗0.3/0/0.3丄寢枌晜庮僗僐傾丗0/0/0)偲偺曬崘偑偁傞(怘埨埾 擾栻昡壙彂 (2018)丄ECHA RAC Opinion (2019)丄CLH Report (2018)丄JMPR (2019)丄擾栻彺榐 (2015))丅 | ||
| 屇媧婍姶嶌惈 | 僨乕僞晄懌偺偨傔暘椶偱偒側偄丅 | ||
| 旂晢姶嶌惈 | (侾)傛傝丄嬫暘1B偲偟偨丅 亂崻嫆僨乕僞亃 (侾)儌儖儌僢僩(n=20)傪梡偄偨Maximisation帋尡(GLP丄旂撪搳梌丗1亾寽戺塼)偵偍偄偰丄24丄48帪娫屻偺梲惈棪偼35亾(7/20椺)丄45亾(9/20椺)偱偁偭偨偲偺曬崘偑偁傞(怘埨埾 擾栻昡壙彂 (2018)丄擾栻彺榐 (2015))丅 亂嶲峫僨乕僞摍亃 (俀)儅僂僗(n=5/孮)傪梡偄偨嬊強儕儞僷愡帋尡(LLNA)(OECD TG 429丄GLP)偵偍偄偰丄巋寖巜悢(SI抣)偼0.78(5亾)丄1.04(10亾)丄0.57(25亾)偱偁偭偨偲偺曬崘偑偁傞(怘埨埾 擾栻昡壙彂 (2018)丄ECHA RAC Opinion (2019)丄CLH Report (2018)丄JMPR (2019)丄擾栻彺榐 (2015))丅 (俁)(俀)偵偮偄偰丄ECHA RAC Opinion (2019)偼帋尡揔梡擹搙傪嵟崅25亾偲偟偨偙偲偵偮偄偰丄梡検愝掕偺梊旛帋尡偵偍偄偰偼50亾偺擹搙偱傕帋尡偝傟偰偄偨偙偲偵怗傟丄OECD TG 429偱掕傔傞梡検愝掕忦審傪枮偨偝側偄壜擻惈偑偁傞偲巜揈偟偰偄傞(ECHA RAC Opinion (2019))丅 | ||
| 惗怋嵶朎曄堎尨惈 | (侾)乣(俈)傛傝丄嬫暘偵奩摉偟側偄丅 亂崻嫆僨乕僞亃 (侾)儅僂僗偺崪悜嵶朎傪梡偄偨彫妀帋尡(GLP)偵偍偄偰堿惈偲偺曬崘偑偁傞(怘埨埾 擾栻昡壙彂 (2018)丄擾栻彺榐 (2015)丄CLH Report (2018)丄RAC (Background Doc.) (2019))丅 (俀)儔僢僩偺娞憻傪梡偄偨晄掕婜DNA崌惉帋尡(GLP)偵偍偄偰堿惈偲偺曬崘偑偁傞(怘埨埾 擾栻昡壙彂 (2018)丄擾栻彺榐 (2015)丄CLH Report (2018)丄RAC (Background Doc.) (2019))丅 (俁)儔僢僩偺娞憻傪梡偄偨僐儊僢僩傾僢僙僀(OECD TG 489丄GLP)偱堿惈偺曬崘偑偁傞(CLH Report (2018)丄RAC (Background Doc.) (2019))丅 (係)儅僂僗偺娞憻傪梡偄偨僐儊僢僩傾僢僙僀偱堿惈偺曬崘偑偁傞(CLH Report (2018)丄RAC (Background Doc.) (2019))丅 (俆)嵶嬠偺暅婣撍慠曄堎帋尡(GLP)偵偍偄偰堿惈偲偺曬崘偑偁傞(怘埨埾 擾栻昡壙彂 (2018)丄擾栻彺榐 (2015))丅 (俇)儅僂僗儕儞僷庮嵶朎傪梡偄偨堚揱巕撍慠曄堎帋尡(GLP)偵偍偄偰堿惈偲偺曬崘偑偁傞(怘埨埾 擾栻昡壙彂 (2018)丄擾栻彺榐 (2015))丅 (俈)傎擕椶攟梴嵶朎(CHL)傪梡偄偨愼怓懱堎忢帋尡偵偍偄偰偼崅擹搙偱梲惈(-S9)偲偺曬崘偑偁傞(CLH Report (2018)丄RAC (Background Doc.) (2019))丅 | ||
| 敪偑傫惈 | (侾)乣(俆)傛傝丄帗梇儔僢僩媦傃帗儅僂僗偺堿惈寢壥暲傃偵梇儅僂僗偺娞憻庮釃偼帺慠敪惗揑側傕偺偲偺敾抐偟丄嬫暘偵奩摉偟側偄丅 亂崻嫆僨乕僞亃 (侾)崙撪奜偺婛懚暘椶寢壥偲偟偰偼丄EPA偱NL(Not Likely To Be Carcinogenic To Humans)偵暘椶偝傟偰偄傞(EPA Annual Cancer Report (2019)丗2011擭暘椶)丅 (俀)儔僢僩傪梡偄偨崿塧搳梌偵傛傞2擭娫敪偑傫惈帋尡偵偍偄偰丄専懱搳梌偵傛傝敪惗昿搙偺憹壛偟偨庮釃惈昦曄偼傒傜傟偢丄敪偑傫惈偼擣傔傜傟側偐偭偨(怘埨埾 擾栻昡壙彂 (2018)丄擾栻彺榐 (2015))丅 (俁)儅僂僗傪梡偄偨78廡娫崿塧搳梌偵傛傞敪偑傫惈帋尡偵偍偄偰丄嵟崅梡検偺5,400 ppm搳梌孮偺梇偱娞嵶朎態庮偲偑傫偺崌寁敪惗昿搙偵桳堄側憹壛偑擣傔傜傟偨(怘埨埾 擾栻昡壙彂 (2018)丄擾栻彺榐 (2015))丅 (係)EPA偼儔僢僩偲儅僂僗偺敪偑傫惈帋尡偱敪偑傫惈偺徹嫆偑側偄偙偲偐傜丄NL偵暘椶偟偨(EPA Pesticide Fact Sheet (2012)丄Federal Register vol. 84, No. 14 (2019))丅 (俆)梇儅僂僗偱偼娞嵶朎態庮偺敪惗昿搙偼懳徠孮偺6亾偵懳偟丄600丄1,800媦傃5,400 ppm偱偼偦傟偧傟13%丄11亾媦傃17%偲梡検憡娭惈偑傒傜傟側偄丅傑偨丄娞偑傫偺昿搙偼摨條偵懳徠孮偺2亾偵懳偟丄偦傟偧傟4亾丄6亾媦傃6亾偱偁傝丄懳徠孮偲搳梌孮偲偺娫偱桳堄嵎偼側偄丅娞嵶朎態庮偲偑傫偺崌寁昿搙偱偼丄梇偺嵟崅搳梌孮(5,400 ppm)偵偍偄偰摑寁揑偵桳堄側嵎偑傒傜傟偨丅偟偐偟丄帋尡巤愝偺攚宨僨乕僞(9.8乣36亾)偺斖埻撪偱偁偭偨(CLH Report (2018)丄RAC (Background Doc.) (2019))丅 | ||
| 惗怋撆惈 | (侾)乣(俁)傛傝丄嬫暘偵奩摉偟側偄丅 亂崻嫆僨乕僞亃 (侾)儔僢僩傪梡偄偨崿塧搳梌偵傛傞擇悽戙惗怋撆惈帋尡(OECD TG 416丄GLP)偵偍偄偰丄P媦傃F1恊摦暔偵堦斒撆惈塭嬁(娞憻丄恡憻丄峛忬態丄寣塼傊偺塭嬁摍)偑傒傜傟傞梡検偱丄帣摦暔偵懱廳憹壛梷惂(F1)丄銪憻廳検掅壓(F2帗)偑傒傜傟偨偑丄斏怋擻偵懳偡傞塭嬁偼擣傔傜傟側偐偭偨偲偺曬崘偑偁傞(怘埨埾 擾栻昡壙彂 (2018)丄擾栻彺榐 (2015)丄CLH Report (2018))丅 (俀)儔僢僩傪梡偄偨嫮惂宱岥搳梌偵傛傞敪惗撆惈帋尡(OECD TG 414丄GLP丄擠怭6乣19擔)偵偍偄偰丄恊摦暔偵娞憻媦傃栍挵廳検偺憹壛偑傒傜傟傞梡検偱丄帣摦暔偵崪奿曄堎戀帣悢偺憹壛偑傒傜傟偨偑丄嵜婏宍惈偼擣傔傜傟側偐偭偨偲偺曬崘偑偁傞(怘埨埾 擾栻昡壙彂 (2018)丄擾栻彺榐 (2015)丄CLH Report (2018))丅 (俁)僂僒僊傪梡偄偨嫮惂宱岥搳梌偵傛傞敪惗撆惈帋尡(OECD TG 414丄GLP丄擠怭6乣27擔)偵偍偄偰丄嵜婏宍惈偼擣傔傜傟側偐偭偨偲偺曬崘偑偁傞(怘埨埾 擾栻昡壙彂 (2018)丄擾栻彺榐 (2015)丄CLH Report (2018))丅 | ||
| 摿掕昗揑憻婍撆惈 (扨夞偽偔業) | (侾)乣(係)傛傝丄嬫暘偵奩摉偟側偄丅 亂崻嫆僨乕僞亃 (侾)儔僢僩傪梡偄偨扨夞宱岥搳梌帋尡(OECD TG 423丄GLP)偵偍偄偰丄2,000 mg/kg(嬫暘2偺斖埻)偱塭嬁偑傒傜傟側偐偭偨偲偺曬崘偑偁傞(怘埨埾 擾栻昡壙彂 (2018)丄CLH Report (2018)丄ECHA RAC Opinion (2019))丅 (俀)儔僢僩傪梡偄偨媫惈恄宱撆惈帋尡(GLP)偵偍偄偰丄2,000 mg/kg(嬫暘2偺斖埻)偱恄宱撆惈偼傒傜傟側偐偭偨偲偺曬崘偑偁傞(怘埨埾 擾栻昡壙彂 (2018))丅 (俁)儔僢僩傪梡偄偨扨夞宱旂搳梌帋尡(OECD TG 402丄GLP)偵偍偄偰丄2,000 mg/kg(嬫暘2偺斖埻)偱峠斄丒醥旂宍惉(専懱揬晅晹埵)傪彍偒丄塭嬁偑傒傜傟側偐偭偨偲偺曬崘偑偁傞(怘埨埾 擾栻昡壙彂 (2018)丄CLH Report (2018)丄ECHA RAC Opinion (2019))丅 (係)儔僢僩傪梡偄偨扨夞媧擖(暡偠傫)偽偔業帋尡(OECD TG 403丄GLP丄4帪娫)偵偍偄偰丄5.18 mg/L(嬫暘奩摉偟側偄斖埻)偱旲晹暘斿暔傪彍偒丄塭嬁偑傒傜傟側偐偭偨偲偺曬崘偑偁傞(怘埨埾 擾栻昡壙彂 (2018)丄CLH Report (2018)丄ECHA RAC Opinion (2019))丅 | ||
| 摿掕昗揑憻婍撆惈 (斀暅偽偔業) | (侾)乣(俈)傛傝丄宱岥丄宱旂宱楬偱偼嬫暘偵奩摉偟側偄丅側偍丄娞憻偵娭楢偡傞強尒偱偁傞ALP忋徃丒娞嵶朎旍戝丄恡憻偵娭楢偡傞強尒偱偁傞枬惈恡徢偼昗揑憻婍偲傒側偣傞塭嬁偱偼側偔丄嵦梡偟偰偄側偄丅偨偩偟丄媧擖宱楬偱偺忣曬偑側偔丄僨乕僞晄懌偺偨傔暘椶偱偒側偄丅 亂崻嫆僨乕僞亃 (侾)儔僢僩傪梡偄偨崿塧搳梌偵傛傞90擔娫宱岥搳梌帋尡(GLP)偵偍偄偰丄2,500 ppm埲忋(150 mg/kg/day(梇)丄171 mg/kg/day(帗)丄嬫暘奩摉偟側偄斖埻)偱娞憻丒恡憻塭嬁(愨懳憡懳廳検憹壛)(梇)丄栍挵塭嬁(愨懳憡懳廳検憹壛)偑傒傜傟偨偲偺曬崘偑偁傞(怘埨埾 擾栻昡壙彂 (2018)丄CLH Report (2018)丄ECHA RAC Opinion (2019))丅 (俀)儔僢僩傪梡偄偨崿塧搳梌偵傛傞2擭娫敪偑傫惈帋尡(GLP)偵偍偄偰丄1,000 ppm埲忋(36.4 mg/kg/day(梇)丄46.5 mg/kg/day(帗)丄嬫暘2偺斖埻)偱枬惈恡徢(帗)偑丄5,000 ppm(197 mg/kg/day(梇)丄245 mg/kg/day(帗)丄嬫暘奩摉偟側偄斖埻)偱恡憻塭嬁(愨懳憡懳廳検憹壛丄枬惈恡徢(梇))丄栍挵塭嬁(愨懳憡懳廳検憹壛丄朿枮)丄娞憻塭嬁(彫梩拞怱惈娞嵶朎帀朾壔丒旍戝丒夡巰丄愨懳憡懳廳検憹壛(帗)丄嬊惈偆偭寣(帗))丄戝挵崟怓撪梕暔(梇)丄挵娫枌儕儞僷愡摯奼挘偑傒傜傟偨偲偺曬崘偑偁傞(怘埨埾 擾栻昡壙彂 (2018)丄CLH Report (2018)丄ECHA RAC Opinion (2019))丅 (俁)儔僢僩傪梡偄偨崿塧搳梌偵傛傞1擭娫宱岥搳梌帋尡(GLP)偵偍偄偰丄1,000 ppm埲忋(42.9 mg/kg/day(梇)丄53.5 mg/kg/day(帗)丄嬫暘2偺斖埻)偱GGT憹壛(帗)偑丄5,000 ppm(226 mg/kg/day(梇)丄275 mg/kg/day(帗)丄嬫暘偵奩摉偟側偄斖埻)偱寣塼塭嬁(Ht丒Hb丒RBC掅壓丄MCV丒MCH丒MCHC掅壓(梇)丄栐愒寣媴悢掅壓(帗))丄PLT憹壛丄APTT墑挿丄TP丒Alb丒Glob憹壛丄栍挵塭嬁(朿枮丄愨懳憡懳廳検憹壛)丄娞憻塭嬁(愨懳憡懳廳検憹壛丄彫梩拞怱惈娞嵶朎旍戝(梇))丄恡憻塭嬁(愨懳憡懳廳検憹壛)丄惛憙忋懱塭嬁(愨懳憡懳廳検憹壛)(梇)丄崪悜憿寣槾恑(梇)丄擜嵶娗岲墫婎惈壔(梇)丄奜堿晹旐栄墭傟(帗)丄棫忋偑傝憹壛(帗)丄A/G斾掅壓(帗)丄T.Chol憹壛(帗)丄擜拞働僩儞懱憹壛(帗)丄怱憻憡懳廳検憹壛(帗)丄擜嵶娗忋旂儕億僼僗僠儞捑拝憹壛(帗)偑傒傜傟偨偲偺曬崘偑偁傞(怘埨埾 擾栻昡壙彂 (2018)丄CLH Report (2018)丄ECHA RAC Opinion (2019))丅 (係)僀僰傪梡偄偨崿塧搳梌偵傛傞90擔娫宱岥搳梌帋尡(GLP)偵偍偄偰丄3,000 ppm埲忋(90.3 mg/kg/day(梇)丄89.8 mg/kg/day(帗)丄嬫暘2偺斖埻)偱ALP忋徃(帗)偑丄15,000 ppm(475 mg/kg/day(帗)丄嬫暘奩摉偟側偄斖埻)偱PLT憹壛(帗)丄彫梩拞怱惈娞嵶朎旍戝(帗)偑丄25,000 ppm(776 mg/kg/day(梇)丄嬫暘奩摉偟側偄斖埻)偱娞憻塭嬁(愨懳憡懳廳検憹壛丒彫梩拞怱惈嵶朎旍戝)(梇)偑傒傜傟偨偲偺曬崘偑偁傞(怘埨埾 擾栻昡壙彂 (2018)丄CLH Report (2018)丄ECHA RAC Opinion (2019))丅 (俆)僀僰傪梡偄偨崿塧搳梌偵傛傞1擭娫宱岥搳梌帋尡(GLP)偵偍偄偰丄3,000 ppm埲忋(83.5 mg/kg/day(梇)丄85.2 mg/kg/day(帗)丄嬫暘2偺斖埻)偱ALP忋徃丄GGT忋徃(帗)偑丄15,000 ppm(448 mg/kg/day(帗)丄嬫暘奩摉偟側偄斖埻)偱娞憡懳廳検憹壛偑丄25,000 ppm(701 mg/kg/day(梇)丄嬫暘奩摉偟側偄斖埻)偱娞憻塭嬁(愨懳憡懳廳検憹壛)偑傒傜傟偨偲偺曬崘偑偁傞(怘埨埾 擾栻昡壙彂 (2018)丄CLH Report (2018)丄ECHA RAC Opinion (2019))丅 (俇)儅僂僗傪梡偄偨崿塧搳梌偵傛傞78廡娫敪偑傫惈帋尡(GLP)偵偍偄偰丄600 ppm埲忋(77.6 mg/kg/day(梇)丄嬫暘2偺斖埻)偱彫梩拞怱惈娞嵶朎旍戝(梇)偑傒傜傟偨偲偺曬崘偑偁傞(怘埨埾 擾栻昡壙彂 (2018)丄CLH Report (2018)丄ECHA RAC Opinion (2019))丅 (俈)儔僢僩傪梡偄偨28擔娫宱旂搳梌帋尡(GLP)偵偍偄偰丄1,000 mg/kg/day(嬫暘奩摉偟側偄斖埻)偱塭嬁偑傒傜傟側偐偭偨偲偺曬崘偑偁傞(CLH Report (2018)丄ECHA RAC Opinion (2019))丅 | ||
| 岆偊傫桳奞惈仏 | 僨乕僞晄懌偺偨傔暘椶偱偒側偄丅 | |||
|---|---|---|---|---|
| *丂JIS Z7252偺夵掶偵傛傝媧堷惈屇媧婍桳奞惈偐傜崁栚柤偑曄峏偲側偭偨丅 | ||||
| 侾俀丏娐嫬塭嬁忣曬 | |||
|---|---|---|---|
| 惗懺撆惈 | |||
| 悈惗娐嫬桳奞惈丂抁婜乮媫惈乯 | 乽憯椶(儉儗儈僇僤僉儌)72帪娫ErC50 = 1.15 mg a.i./L(悈嶻摦怉暔偺旐奞杊巭偵學傞擾栻搊榐曐棷婎弨偺愝掕偵娭偡傞帒椏, 2012)偱偁傞偙偲偐傜丄嬫暘2偲偟偨丅(a.i.: active ingredient)乿 | ||
| 悈惗娐嫬桳奞惈丂挿婜乮枬惈乯 | 媫懍暘夝惈偵娭偡傞廫暘側僨乕僞偑摼傜傟偰偄側偄丅峛妅椶(僆僆儈僕儞僐)偺21擔娫NOEC = 0.0899 mg/L(EU CLP CLH, 2018)偐傜丄嬫暘1偲偟偨丅 | ||
| 巆棷惈丒暘夝惈 | 忣曬側偟 | ||
| 惗懺拁愊惈 | 忣曬側偟 | ||
| 搚忞拞偺堏摦惈 | 忣曬側偟 | ||
| 僆僝儞憌傊偺桳奞惈 | 摉奩暔幙偼儌儞僩儕僆乕儖媍掕彂偺晬懏彂偵楍婰偝傟偰偄側偄偨傔丅 | ||
| 侾俁丏攑婞忋偺拲堄 | |||
|---|---|---|---|
| 壔妛昳乮巆梋攑婞暔乯丄摉奩壔妛昳偑晅拝偟偰偄傞墭愼梕婍媦傃曪憰偺埨慡偱丄偐偮丄娐嫬忋朷傑偟偄攑婞丄枖偼儕僒僀僋儖偵娭偡傞忣曬 | 攑婞偵偍偄偰偼丄娭楢朄婯側傜傃偵抧曽帺帯懱偺婎弨偵廬偆偙偲丅 搒摴晎導抦帠側偳偺嫋壜傪庴偗偨嶻嬈攑婞暔張棟嬈幰丄傕偟偔偼抧曽岞嫟抍懱偑偦偺張棟傪峴偭偰偄傞応崌偵偼偦偙偵埾戸偟偰張棟偡傞丅 攑婞暔偺張棟傪埾戸偡傞応崌丄張棟嬈幰摍偵婋尟惈丄桳奞惈傪廫暘崘抦偺忋張棟傪埾戸偡傞丅 梕婍偼愻忩偟偰儕僒僀僋儖偡傞偐丄娭楢朄婯惂暲傃偵抧曽帺帯懱偺婎弨偵廬偭偰揔愗側張暘傪峴偆丅 嬻梕婍傪攑婞偡傞応崌偼丄撪梕暔傪姰慡偵彍嫀偡傞偙偲丅 | ||
| 侾係丏桝憲忋偺拲堄 | ||||
|---|---|---|---|---|
| 杮暔幙偺GHS暘椶寢壥偵婎偯偔崙嵺婯惂偺暘椶摍偼丄埲壓偺捠傝偲悇掕偝傟傞偑丄奩斲偼惢昳偵傛偭偰堎側傞応崌偑偁傞丅桝憲婋尟暔偺暘椶偼丄梕婍摍媺傪娷傔丄壸憲恖偑愑擟傪傕偭偰敾抐偡傞偙偲偲偝傟偰偄傞偨傔丄桝憲偺嵺偵偼丄屄乆偺壿暔偵偮偄偰丄惢昳偺忬懺丄宍忬摍傕峫椂偟丄桝憲儌乕僪 (峲嬻丄慏敃) 傪婯惂偡傞朄婯偵増偭偰帠嬈幰偑敾抐偡傞昁梫偑偁傞丅 | ||||
| 崙嵺婯惂 | ||||
| 崙楢斣崋 | 3077 | |||
| 昳柤乮崙楢桝憲柤乯 | 娐嫬桳奞暔幙丄屌懱丄懠偵昳柤偑柧帵偝傟偰偄側偄傕偺 | |||
| 崙楢暘椶 | 9 | |||
| 暃師婋尟 | - | |||
| 梕婍摍媺 | III | |||
| 奀梞墭愼暔幙 | 奩摉偡傞 | |||
| MARPOL73/78晬懏彂嘦媦傃IBC僐乕僪偵傛傞偽傜愊傒桝憲偝傟傞塼懱暔幙 | 奩摉偟側偄 | |||
| 崙撪婯惂 | ||||
| 奀忋婯惂忣曬 | 慏敃埨慡朄偺婯掕偵廬偆 | |||
| 峲嬻婯惂忣曬 | 峲嬻朄偺婯掕偵廬偆 | |||
| 棨忋婯惂忣曬 | 奩摉偟側偄 | |||
| 摿暿側埨慡忋偺懳嶔 | 奩摉偟側偄 | |||
| 偦偺懠 (堦斒揑) 拲堄 | 桝憲偵嵺偟偰偼丄捈幩擔岝傪旔偗丄梕婍偺攋懝丄晠怘丄楻傟偺側偄傛偆偵愊傒崬傒丄壸曵傟偺杊巭傪妋幚偵峴偆丅 廳検暔傪忋愊傒偟側偄丅 | |||
| 嬞媫帪墳媫慬抲巜恓斣崋* | 171 | |||
| *丂杒暷嬞媫帪墳媫慬抲巜恓偵婎偯偔丅暷崙塣桝徣偑拞怱偲側偭偰敪峴偟偨乽2024 Emengency Response Guidebook乿偵宖嵹偝傟偰偄傞丅 | ||||
| 侾俆丏揔梡朄椷 | ||||
|---|---|---|---|---|
| 朄婯惂忣曬偼嶌惉擭寧擔帪揰偵婎偯偄偰婰嵹偝傟偰偍傝傑偡丅帠嬈応偵偍偄偰婰嵹偡傞偵摉偨偭偰偼丄嵟怴忣曬傪妋擣偟偰偔偩偝偄丅 | ||||
| 楯摥埨慡塹惗朄 | 旂晢摍忈奞壔妛暔幙(楯摥埨慡塹惗婯懃戞俆俋係忦偺俀) | |||
| 壔妛暔幙攔弌攃埇娗棟懀恑朄 (PRTR朄) | 戞擇庬巜掕壔妛暔幙(朄戞俀忦戞俁崁丄巤峴椷戞俀忦暿昞戞俀)亂俁係丂乮俆亅僋儘儘亅俀亅儊僩僉僔亅係亅儊僠儖僺儕僕儞亅俁亅僀儖乯乮俀丆俁丆係亅僩儕儊僩僉僔亅俇亅儊僠儖僼僃僯儖乯儊僞僲儞乮暿柤僺儕僆僼僃僲儞乯亃 | |||
| 撆暔媦傃寑暔庢掲朄 | - | |||
| 悈摴朄 | 悈幙婎弨(暯侾俆徣椷侾侽侾崋) 亂俁俉丂墫壔暔僀僆儞亃 | |||
| 慏敃埨慡朄 | 桳奞惈暔幙(婋婯懃戞俁忦婋尟暔崘帵暿昞戞侾) | |||
| 峲嬻朄 | 桳奞惈暔幙(巤峴婯懃戞侾俋係忦婋尟暔崘帵暿昞戞侾) | |||
| 侾俇丏偦偺懠偺忣曬 | ||||
|---|---|---|---|---|
| 嶲峫暥專 | ||||
| 9崁丄11崁偵偮偄偰偼奺僨乕僞枅偵婰嵹粋虘紓虋e崁偵偮偄偰偼埲壓傪嶲徠丅 丒NITE壔妛暔幙憤崌忣曬採嫙僔僗僥儉乮NITE-CHRIP乯 丒International Chemical Safety Cards (ICSC) 丒Hazardous Substances Data Bank (HSDB) 丒GESTIS Substance database (GESTIS) 丒2024 Emengency Response Guidebook 丒堦斒幮抍朄恖擔杮壔妛岺嬈嫤夛 曇乽GHS懳墳僈僀僪儔僀儞 儔儀儖媦傃昞帵丒埨慡僨亅僞僔亅僩嶌惉巜恓乿 丒岤惗楯摥徣乽旂晢忈奞摍杊巭梡曐岇嬶偺慖掕儅僯儏傾儖戞侾斉乿 | ||||