| 1.化学品及び会社情報 | |||
|---|---|---|---|
| 化学品の名称 | イソニアジド(Isoniazid) | ||
| 製品コード | 23A5063 | ||
| 会社名 | ○○○○株式会社 | ||
| 住所 | 東京都△△区△△町△丁目△△番地 | ||
| 電話番号 | 03-1234-5678 | ||
| FAX番号 | 03-1234-5678 | ||
| 電子メールアドレス | 連絡先@検セ.or.jp | ||
| 緊急時の電話番号 | 03-1234-5678 | ||
| 推奨用途及び使用上の制限 | 抗結核剤 | ||
| 2.危険有害性の要約 | ||||
|---|---|---|---|---|
| GHS分類 | ||||
| 分類実施日 | H24.3.1、政府向けGHS分類ガイダンス(H22.7月版)を使用 | |||
| 環境に対する有害性はGHS改訂4版を使用 | ||||
| 健康に対する有害性 | 急性毒性(経口) | 区分4 | ||
| 生殖毒性 | 区分2 | |||
| 特定標的臓器毒性(単回ばく露) | 区分1(神経系) | |||
| 特定標的臓器毒性(反復ばく露) | 区分1(神経系、肝臓、血液) | |||
| 環境に対する有害性 | 水生環境有害性 (急性) | 区分3 | ||
| 水生環境有害性 (長期間) | 区分3 | |||
| 注) 上記のGHS分類で区分の記載がない危険有害性項目については、政府向けガイダンス文書で規定された「分類対象外」、「区分外」または「分類できない」に該当する。なお、健康有害性については後述の11項に、環境有害性については12項に、「分類対象外」、「区分外」または「分類できない」の記述がある。 | ||||
| GHSラベル要素 | ||||
| 絵表示 |   | |||
| 注意喚起語 | 危険 | |||
| 危険有害性情報 | 飲み込むと有害 | |||
| 生殖能又は胎児への悪影響のおそれの疑い | ||||
| 臓器の障害(神経系) | ||||
| 長期にわたる、又は反復ばく露による臓器の障害(神経系、肝臓、血液) | ||||
| 長期継続的影響により水生生物に毒性 | ||||
| 注意書き | ||||
| 安全対策 | 使用前に取扱説明書を入手すること。 | |||
| すべての安全注意を読み理解するまで取り扱わないこと。 | ||||
| 粉じん、煙、ガス、ミスト、蒸気、スプレーを吸入しないこと。 | ||||
| 取扱後は手などをよく洗うこと。 | ||||
| この製品を使用する時に、飲食又は喫煙をしないこと。 | ||||
| 環境への放出を避けること。 | ||||
| 保護手袋、保護衣、保護眼鏡、保護面を着用すること。 | ||||
| 応急措置 | 飲み込んだ場合:気分が悪いときは医師に連絡すること。 | |||
| 口をすすぐこと。 | ||||
| 気分が悪いときは、医師の診断、手当てを受けること。 | ||||
| ばく露又はばく露の懸念がある場合:医師の診断、手当てを受けること。 | ||||
| 特別な処置が必要である。(このラベルの…を見よ。) | ||||
| 保管 | 施錠して保管すること。 | |||
| 廃棄 | 内容物、容器を都道府県知事の許可を受けた専門の廃棄物処理業者に委託すること。 | |||
| 3.組成及び成分情報 | |||
|---|---|---|---|
| 単一製品・混合物の区別 | 単一製品 | ||
| 化学名又は一般名 | イソニアジド | ||
| 別名 | ピリジン-4-カルボン酸ヒドラジド、イソニコチン酸ヒドラジド、ヒドラソニル、Pyridine-4-carboxylic acid hydrazide、Isonicotinic acid hydrazide、Hidrasonil | ||
| 濃度又は濃度範囲 | 100% | ||
| 分子式 (分子量) | C6H7N3O(137.142) | ||
| 化学特性 (示性式又は構造式) | 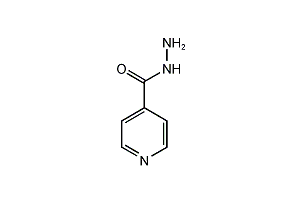 | ||
| CAS番号 | 54-85-3 | ||
| 官報公示整理番号(化審法) | (5)-737 | ||
| 官報公示整理番号(安衛法) | (5)-737 | ||
| 分類に寄与する不純物及び安定化添加物 | データなし。 | ||
| 4.応急措置 | |||
|---|---|---|---|
| 吸入した場合 | 新鮮な空気、安静。 | ||
| 気分が悪いときは、医師の診断、手当てを受けること。 | |||
| ばく露又はばく露の懸念がある場合:医師の診断、手当てを受けること。 | |||
| 特別な処置が必要である。(このラベルの…を見よ。) | |||
| 皮膚に付着した場合 | 汚染された衣服を脱がせる。洗い流してから水と石鹸で皮膚を洗浄する。 | ||
| 皮膚刺激が生じた場合:医師の診断、手当てを受けること。 | |||
| 気分が悪いときは、医師の診断、手当てを受けること。 | |||
| ばく露又はばく露の懸念がある場合:医師の診断、手当てを受けること。 | |||
| 特別な処置が必要である。(このラベルの…を見よ。) | |||
| 眼に入った場合 | 水で数分間注意深く洗うこと。次にコンタクトレンズを着用していて容易に外せる場合は外すこと。その後も洗浄を続けること。 | ||
| 気分が悪いときは、医師の診断、手当てを受けること。 | |||
| ばく露又はばく露の懸念がある場合:医師の診断、手当てを受けること。 | |||
| 特別な処置が必要である。(このラベルの…を見よ。) | |||
| 飲み込んだ場合 | 気分が悪いときは医師に連絡すること。 | ||
| 口をすすぐ。水に活性炭を懸濁した液を飲ませる。医療機関に連絡する。 | |||
| ばく露又はばく露の懸念がある場合:医師の診断、手当てを受けること。 | |||
| 特別な処置が必要である。(このラベルの…を見よ。) | |||
| 予想される急性症状及び遅発性症状の最も重要な兆候及び症状 | 吸入:データなし。 | ||
| 皮膚:データなし。 | |||
| 眼:データなし。 | |||
| 経口摂取:錯乱、痙攣、吐き気、脱力感、運動失調、幻覚。 | |||
| 応急措置をする者の保護 | 粉塵の拡散を防ぐ! | ||
| 医師に対する特別注意事項 | 神経系、腎臓に影響を与え、見当識障害、し眠、昏睡、代謝性アシドーシスを起こすことがある。高濃度の場合、死に至ることがある。意識を喪失することがある。 | ||
| 中枢神経系、肝臓に影響を与え、組織損傷、機能障害を生じることがある。 | |||
| 5.火災時の措置 | |||
|---|---|---|---|
| 消火剤 | 水噴霧、粉末消火薬剤、泡消火剤、二酸化炭素 | ||
| 使ってはならない消火剤 | 情報なし。 | ||
| 特有の危険有害性 | 当該製品は分子中にNを含有しているため火災時に刺激性もしくは有毒なヒューム(またはガス)を放出する。 | ||
| 当該製品は分子中にNを含有しているため燃焼ガスには、一酸化炭素などの他、窒素酸化物系のガスなどの有毒ガスが含まれるので、消火作業の際には、煙を吸入しないように注意する。 | |||
| 特有の消火方法 | 消火作業は、風上から行う。 | ||
| 周辺火災の場合に移動可能な容器は、速やかに安全な場所に移す。 | |||
| 火災発生場所の周辺に関係者以外の立入りを禁止する。 | |||
| 関係者以外は安全な場所に退去させる。 | |||
| 消火を行う者の保護 | 消火作業では、適切な保護具(手袋、眼鏡、マスク等)を着用する。 | ||
| 6.漏出時の措置 | |||
|---|---|---|---|
| 人体に対する注意事項、保護具及び緊急措置 | 作業には、必ず保護具(手袋・眼鏡・特別個人用保護具:P2有害粒子用フィルター付マスクなど)を着用する。 | ||
| 多量の場合、人を安全な場所に退避させる。 | |||
| 必要に応じた換気を確保する。 | |||
| 環境に対する注意事項 | 漏出物を河川や下水に直接流してはいけない。 | ||
| 封じ込め及び浄化の方法及び機材 | 漏出したものをすくいとり、または掃き集めて紙袋またはドラムなどに回収する。 | ||
| 粉末の場合は、電気掃除機(真空クリーナー)、ほうきなどを使用して回収する。 | |||
| 湿らせてもよい場合は、粉塵を避けるために湿らせてから掃き入れる。 | |||
| 残留分を注意深く集め、安全な場所に移す。 | |||
| 付近の着火源となるものを速やかに除くとともに消火剤を準備する。 | |||
| 床に漏れた状態で放置すると、滑り易くスリップ事故の原因となるため注意する。 | |||
| 漏出物の上をむやみに歩かない。 | |||
| 火花を発生しない安全な用具を使用する。 | |||
| 7.取扱い及び保管上の注意 | |||
|---|---|---|---|
| 取扱い | |||
| 技術的対策 | 取扱い場所の近くに、洗眼及び身体洗浄のための設備を設置する。 | ||
| 安全取扱い注意事項 | 使用前に取扱説明書を入手すること。 | ||
| すべての安全注意を読み理解するまで取り扱わないこと。 | |||
| 粉じん、煙、ガス、ミスト、蒸気、スプレーを吸入しないこと。 | |||
| 取扱後は手などをよく洗うこと。 | |||
| この製品を使用する時に、飲食又は喫煙をしないこと。 | |||
| 環境への放出を避けること。 | |||
| 保護手袋、保護衣、保護眼鏡、保護面を着用すること。 | |||
| 裸火禁止。 | |||
| 粉塵の拡散を防ぐ! | |||
| 局所排気または呼吸用保護具。 | |||
| 保護手袋。 | |||
| 安全眼鏡。 | |||
| 作業中は飲食、喫煙をしない。 | |||
| 20℃ではほとんど気化しない;しかし、とくに粉末の場合拡散すると浮遊粒子が急速に有害濃度に達することがある。 | |||
| 衛生対策 | 取扱い後は手などをよく洗うこと。 | ||
| 保管 | |||
| 安全な保管条件 | 換気の良い場所で保管すること。 | ||
| 施錠して保管すること。 | |||
| 窒素シールをして保管する。酸性物質と一緒に保管しない。 | |||
| 容器包装材料 | 鉄製の容器はさける。 | ||
| 8.ばく露防止及び保護措置 | |||
|---|---|---|---|
| 管理濃度 | 未設定 | ||
| 許容濃度 | |||
| 日本産衛学会(2010年度版) | 未設定 | ||
| ACGIH(2011年版) | 未設定 | ||
| 設備対策 | 蒸気、ヒューム、ミストまたは粉塵が発生する場合は、局所排気装置を設置する。 | ||
| 取扱い場所の近くに、洗眼及び身体洗浄のための設備を設置する。 | |||
| 保護具 | |||
| 呼吸器の保護具 | 適切な呼吸器用保護具を着用すること。 | ||
| 手の保護具 | 適切な保護手袋を着用すること。 | ||
| 眼の保護具 | 適切な眼の保護具を着用すること。 | ||
| 皮膚及び身体の保護具 | 適切な保護手袋、保護衣、保護眼鏡、保護面を着用すること。 | ||
| 9.物理的及び化学的性質 | |||
|---|---|---|---|
| 物理的状態 | |||
| 形状 | 結晶(Ullmanns(E) (6th, 2003)) | ||
| 色 | 無色または白色(HSDB (2005)) | ||
| 臭い | 無臭(GESTIS(Access on May. 2011)) | ||
| 臭いのしきい(閾)値 | データなし。 | ||
| pH | 6−8(20℃、濃度:50g/L)(GESTIS(Access on May. 2011)) | ||
| 融点・凝固点 | 171.4℃(Merck (14th, 2006)) | ||
| 沸点、初留点及び沸騰範囲 | データなし。 | ||
| 引火点 | > 250℃(不明)(GESTIS(Access on May. 2011)) | ||
| 蒸発速度(酢酸ブチル=1) | データなし。 | ||
| 燃焼性(固体、気体) | データなし。 | ||
| 燃焼又は爆発範囲 | データなし。 | ||
| 蒸気圧 | 0.0000464mmHg(25℃)(Howard (1997)) | ||
| 蒸気密度 | データなし。 | ||
| 比重(相対密度) | データなし。 | ||
| 溶解度 | 水:140000 mg/L at 25 deg C (HSDB (2005)) | ||
| エタノールに可溶、エーテルに不溶(有機化合物辞典 (1985)) | |||
| n-オクタノール/水分配係数 | log Kow = -0.70(HSDB (2005)) | ||
| 自然発火温度 | データなし。 | ||
| 分解温度 | データなし。 | ||
| 粘度(粘性率) | データなし。 | ||
| 10.安定性及び反応性 | |||
|---|---|---|---|
| 反応性 | 情報なし。 | ||
| 安定性 | 情報なし。 | ||
| 危険有害反応可能性 | データなし。 | ||
| 避けるべき条件 | データなし。 | ||
| 混触危険物質 | データなし。 | ||
| 危険有害な分解生成物 | データなし。 | ||
| 11.有害性情報 | |||
|---|---|---|---|
| 急性毒性 | |||
| 経口 | ラットのLD50値は650 mg/kg bw(PIM 288 (1999))である。GHS分類:区分4 | ||
| 経皮 | データなし。GHS分類:分類できない | ||
| 吸入:ガス | GHSの定義における固体である。GHS分類:分類対象外 | ||
| 吸入:蒸気 | データなし。GHS分類:分類できない | ||
| 吸入:粉じん及びミスト | データなし。GHS分類:分類できない | ||
| 皮膚腐食性及び刺激性 | データなし。GHS分類:分類できない | ||
| 眼に対する重篤な損傷性又は眼刺激性 | データなし。GHS分類:分類できない | ||
| 呼吸器感作性 | データなし。GHS分類:分類できない | ||
| 皮膚感作性 | データなし。GHS分類:分類できない | ||
| 生殖細胞変異原性 | マウスを用いた優性致死試験(生殖細胞in vivo経世代変異原性試験)で陰性(IARC suppl. 7 (1987))、本物質で治療されたヒトのリンパ球を用いた染色体異常試験およびげっ歯類を用いた染色体異常試験(in vivo変異原性試験)でいずれも陰性(IARC suppl. 7 (1987))の報告がある。なお、げっ歯類を用いた姉妹染色分体交換試験とDNA損傷試験(in vivo遺伝毒性試験)の結果も陰性であった(IARC suppl. 7 (1987))が、in vitro試験としてエームス試験とげっ歯類の培養細胞を用いた染色体異常試験では陽性(IARC suppl. 7 (1987))が報告されている。GHS分類:区分外 | ||
| 発がん性 | IARCによる発がん性評価でグループ3に分類されている(IARC suppl.7 (1987))。なお、動物試験データとして、混餌または飲水での経口投与により、マウスで肺腫瘍の発生率が用量依存的に増加したが、ラットでは腫瘍の発生増加は明確でなく、ハムスターでは有意な影響は見られなかった(IARC 4 (1974))。また、ヒトで大規模な疫学調査の結果、肺腫瘍による死亡および肺腫瘍の発生率の統計学的に有意な増加はなく、また、癌による死亡の発生頻度の増加も認められなかった(IARC 4 (1974))。GHS分類:分類できない | ||
| 生殖毒性 | 妊娠期間の最初3〜4ヵ月にばく露を受けた母親の乳児における奇形発生率の増加や重度の脳症、自殺企図のため大量摂取した母親からの先天性多発性関節拘縮症候群を有する死亡児の出産(Birth Defects (3rd, 2000))、さらに85人の母親から10人の奇形児の出産(Teratogenic (12th, 2007))など、ヒトで児の発生に対する悪影響の報告がいくつかある。なお、妊娠または妊娠している可能性のある婦人には投与しないことが望ましい(マウスで胎児の発育障害が認められている)との記載がある(医療用医薬品集 (2010))。また、本物質は乳汁中に排出されるが、乳汁中濃度も低い(HSDB (2005))ことから、授乳に対するまたは授乳を介した影響は分類の根拠としなかった。GHS分類:区分2 | ||
| 特定標的臓器毒性(単回ばく露) | ばく露による急性影響として、30〜40 mg/kgの用量で痙攣発作が見られ、発作障害の既往がある大人では14 mg/kgの低用量でも発現する(PIM 288 (1999))との記述、また、嘔気、嘔吐のほか、視力異常、眩暈、言語障害などの初期症状に続き、次の段階には重度の大発作痙攣、呼吸窮迫、昏睡などが急速に現れる(PIM 288 (1999))との記述がある。GHS分類:区分1(神経系) | ||
| 特定標的臓器毒性(反復ばく露) | 本物質は医薬品の結核化学療法剤として使用され(医療用医薬品集 (2010))、長期投与で最も頻繁に現れる副作用は末梢神経障害と肝毒性である(PIM 288 (1999))と記述されている。末梢神経障害の素因にアルコール、栄養失調、妊娠などがあり、発現は用量依存的で5 mg/kg/日では稀であるが300 mg/kg/日になると頻繁になる(PIM 288 (1999))との記述がある。GHS分類:区分1(神経系) 一方、患者の10〜20%に無症候性の血清GOTの上昇がみられ、黄疸を伴う肝炎発生(0.5%)の可能性があり、その発生は大抵の場合投与開始後3ヵ月以内である(PIM 288 (1999))との記述がある。GHS分類:区分1(肝臓) さらに、その他の主な副作用として、汎発性血管内凝固症候群、顆粒球増加症、貧血、血小板減少などが記載されている(PIM 288 (1999))。GHS分類:区分1(血液)となる。 | ||
| 吸引性呼吸器有害性 | データなし。GHS分類:分類できない | ||
| 12.環境影響情報 | |||
|---|---|---|---|
| 生態毒性 | |||
| 水生環境有害性(急性) | 甲殻類(オオミジンコ)の24時間EC50 = 84.6 mg/L (AQUIRE, 2012) から、区分3とした。GHS分類:区分3 | ||
| 水生環境有害性(長期間) | 信頼性のある慢性毒性データが得られていない。急速分解性がなく(BIOWIN)、急性毒性区分3であることから、区分3とした。GHS分類:区分3 | ||
| オゾン層への有害性 | 当該物質はモントリオール議定書の附属書に列記されていないため。GHS分類:分類できない | ||
| 13.廃棄上の注意 | |||
|---|---|---|---|
| 残余廃棄物 | 廃棄の前に、可能な限り無害化、安定化及び中和等の処理を行って危険有害性のレベルを低い状態にする。 | ||
| 内容物/容器を都道府県知事の許可を受けた専門の廃棄物処理業者に委託すること。 | |||
| 汚染容器及び包装 | 容器は清浄にしてリサイクルするか、関連法規並びに地方自治体の基準に従って適切な処分を行う。 | ||
| 空容器を廃棄する場合は、内容物を完全に除去すること。 | |||
| 14.輸送上の注意 | ||||
|---|---|---|---|---|
| 該当の有無は製品によっても異なる場合がある。法規に則った試験の情報に基づく修正の必要がある。 | ||||
| 国際規制 | 海上輸送はIMOの規則に、航空輸送はICAO/IATAの規則に従う。 | |||
| 国連番号 | 特定できず。 | |||
| 海洋汚染物質 | 該当しない。 | |||
| 国内規制 | ||||
| 海上規制情報 | 船舶安全法の規定に従う。 | |||
| 航空規制情報 | 航空法の規定に従う。 | |||
| 陸上規制情報 | 該当しない。 | |||
| 特別安全対策 | 移送時にイエローカードの保持が必要。 | |||
| 食品や飼料と一緒に輸送してはならない。 | ||||
| 輸送に際しては、直射日光を避け、容器の破損、腐食、漏れのないように積み込み、荷崩れの防止を確実に行う。 | ||||
| 重量物を上積みしない。 | ||||
| 15.適用法令 | ||||
|---|---|---|---|---|
| 法規制情報は作成年月日時点に基づいて記載されております。事業場において記載するに当たっては、最新情報を確認してください。 | ||||
| 船舶安全法 | 毒物類・毒物 | |||
| 航空法 | 毒物類・毒物 | |||
| 16.その他の情報 | ||||
|---|---|---|---|---|
| 参考文献 | 各データ毎に記載した。 | |||
| <モデルSDSを利用するときの注意事項> 本モデルデータシートは作成年月日時点における情報に基づいて記載されておりますので、事業場においてSDSを作成するに当たっては、新たな危険有害性情報について確認することが必要です。さらに、本データシートはモデルですので、実際の製品等の性状に基づき追加修正する必要があります。また、特殊な条件下で使用するときは、その使用状況に応じた情報に基づく安全対策が必要となります。 | ||||