| 1.化学品等及び会社情報 | |||
|---|---|---|---|
| 化学品等の名称 | (SP‐4‐2)‐ジアンミンジクロロ白金(別名:シスプラチン) | ||
| 製品コード | H30-C-023-MHLW | ||
| 会社名 | ○○○○株式会社 | ||
| 住所 | 東京都△△区△△町△丁目△△番地 | ||
| 電話番号 | 03-1234-5678 | ||
| ファックス番号 | 03-1234-5678 | ||
| 電子メールアドレス | 連絡先@検セ.or.jp | ||
| 緊急連絡電話番号 | 03-1234-5678 | ||
| 推奨用途及び使用上の制限 | 医薬(抗悪性腫瘍剤) | ||
| 2.危険有害性の要約 | ||||
|---|---|---|---|---|
| GHS分類 | ||||
| 分類実施日 (物化危険性及び健康有害性) | H31.3.15、政府向けGHS分類ガイダンス (H25年度改訂版 (ver1.1):JIS Z7252:2014準拠) を使用 | |||
| GHS改訂4版を使用 | ||||
| 物理化学的危険性 | - | |||
| 健康に対する有害性 | 急性毒性(経口) | 区分2 | ||
| 眼に対する重篤な損傷性又は眼刺激性 | 区分2A | |||
| 生殖細胞変異原性 | 区分1B | |||
| 発がん性 | 区分1B | |||
| 生殖毒性 | 区分1B、追加区分:授乳に対するまたは授乳を介した影響 | |||
| 特定標的臓器毒性 (単回ばく露) | 区分1(消化器、骨髄、腎臓、神経系) | |||
| 特定標的臓器毒性 (反復ばく露) | 区分1(骨髄、腎臓、神経系、消化器系、全身毒性) | |||
| 分類実施日 (環境有害性) | 環境に対する有害性はH18年度、GHS分類マニュアル(H18.2.10版)を使用 | |||
| 環境に対する有害性 | - | |||
| 注) 上記のGHS分類で区分の記載がない危険有害性項目については、政府向けガイダンス文書で規定された「分類対象外」、「区分外」又は「分類できない」に該当する。なお、これらに該当する場合は後述の11項に記載した。 | ||||
| GHSラベル要素 | ||||
| 絵表示 |   | |||
| 注意喚起語 | 危険 | |||
| 危険有害性情報 | 飲み込むと生命に危険 強い眼刺激 遺伝性疾患のおそれ 発がんのおそれ 生殖能又は胎児への悪影響のおそれ 授乳中の子に害を及ぼすおそれ 消化器、骨髄、腎臓、神経系の障害 長期にわたる又は反復ばく露による骨髄、腎臓、神経系、消化器系、全身の障害 | |||
| 注意書き | ||||
| 安全対策 | 取扱い後は...よく洗うこと。 この製品を使用する時に、飲食又は喫煙をしないこと。 保護手袋/保護衣/保護眼鏡/保護面を着用すること。 使用前に取扱説明書を入手すること。 全ての安全注意を読み理解するまで取り扱わないこと。 粉じん/煙/ガス/ミスト/蒸気/スプレーを吸入しないこと。 妊娠中/授乳期中は接触を避けること。 | |||
| 応急措置 | 飲み込んだ場合:直ちに医師に連絡すること。 特別な処置が必要である (このラベルの...を見よ)。注) ”…”は、ラベルに解毒剤等中毒時の情報提供を受けるための連絡先などが記載されている場合のものです。ラベル作成時には、”…”を適切に置き換えてください。 口をすすぐこと。 眼に入った場合:水で数分間注意深く洗うこと。次にコンタクトレンズを着用していて容易に外せる場合は外すこと。その後も洗浄を続けること。 眼の刺激が続く場合:医師の診断/手当てを受けること。 ばく露またはばく露の懸念がある場合:医師の診断/手当を受けること。 気分が悪いときは、医師の診断/手当てを受けること。 | |||
| 保管 | 施錠して保管すること。 | |||
| 廃棄 | 内容物/容器を都道府県知事の許可を受けた専門の廃棄物処理業者に依頼して廃棄すること。 | |||
| 他の危険有害性 | - | |||
| 3.組成及び成分情報 | |||
|---|---|---|---|
| 単一製品・混合物の区別 | 単一製品 | ||
| 化学名又は一般名 | (SP−4−2)−ジアンミンジクロロ白金 | ||
| 別名 | シスプラチン cis−ジアンミンジクロロ白金 cis-Diamminedichloroplatinum(II) cis-Dichlorodiammineplatinum(II) Etoposide in combination with cisplatin and bleomycin Platinum, diamminedichloro-, (SP-4-2)- | ||
| 濃度又は濃度範囲 | 100% | ||
| 分子式 (分子量) | Cl2H6N2Pt (-) | ||
| 化学特性 (示性式又は 構造式) | 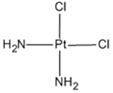 | ||
| CAS番号 | 15663-27-1 | ||
| 官報公示整理番号 (化審法) | 情報なし | ||
| 官報公示整理番号 (安衛法) | 情報なし | ||
| 分類に寄与する不純物及び 安定化添加物 | - | ||
| 4.応急措置 | 「2.危険有害性の要約」における応急措置も確認すること。 | ||
|---|---|---|---|
| 吸入した場合 | 気分が悪い時は、医師の診断、手当てを受けること。 | ||
| 皮膚に付着した場合 | 水と石鹸で洗うこと。 皮膚刺激が生じた場合、医師の診断、手当てを受けること。 | ||
| 眼に入った場合 | 水で数分間注意深く洗うこと。次にコンタクトレンズを着用していて容易に外せる場合は外すこと。その後も洗浄を続けること。 眼の刺激が続く場合:医師の診断、手当てを受けること。 | ||
| 飲み込んだ場合 | 直ちに医師に連絡すること。 口をすすぐこと。 | ||
| 急性症状及び遅発性症状の最も重要な徴候症状 | 吸入 : データなし 皮膚 : データなし 眼 : データなし 経口摂取 : データなし | ||
| 応急措置をする者の保護 | データなし | ||
| 医師に対する特別な注意事項 | データなし | ||
| 5.火災時の措置 | |||
|---|---|---|---|
| 消火剤 | 水噴霧、泡消火剤、粉末消火剤、炭酸ガス、乾燥砂類 | ||
| 使ってはならない消火剤 | 棒状放水 | ||
| 特有の危険有害性 | 不燃性であり、それ自身は燃えないが、加熱されると分解して、腐食性及び/又は毒性の煙霧を発生するおそれがある。 火災時に刺激性、腐食性及び毒性のガスを発生するおそれがある。 | ||
| 特有の消火方法 | 危険でなければ火災区域から容器を移動する。 | ||
| 消火を行う者の保護 | 適切な空気呼吸器、防護服(耐熱性)を着用する。 | ||
| 6.漏出時の措置 | |||
|---|---|---|---|
| 人体に対する注意事項、保護具及び 緊急措置 | 情報なし | ||
| 環境に対する注意事項 | 情報なし | ||
| 封じ込め及び浄化の方法及び機材 | 情報なし | ||
| 7.取扱い及び保管上の注意 | |||
|---|---|---|---|
| 取扱い | |||
| 技術的対策 | 『8.ばく露防止及び保護措置』に記載の設備対策を行い、保護具を着用する。 | ||
| 安全取扱い注意事項 | 取扱後は手をよく洗うこと。 この製品を使用する時に、飲食または喫煙をしないこと。 適切な保護眼鏡、保護面を着用すること。 使用前に取扱説明書を入手すること。 全ての安全注意を読み理解するまで取り扱わないこと。 適切な個人用保護具を使用すること。 粉じん、ヒューム、蒸気、スプレーを吸入しないこと。 妊娠中、授乳期中は接触を避けること。 | ||
| 接触回避 | 情報なし | ||
| 衛生対策 | 情報なし | ||
| 保管 | |||
| 安全な保管条件 | 情報なし | ||
| 安全な容器包装材料 | データなし | ||
| 8.ばく露防止及び保護措置 | |||
|---|---|---|---|
| 管理濃度 | 未設定 | ||
| 許容濃度 | |||
| 日本産衛学会(2019年度版) | 未設定 | ||
| ACGIH(2019年度版) | 未設定 | ||
| 設備対策 | この物質を貯蔵ないし取扱う作業場には洗眼器と安全シャワーを設置すること。 ばく露を防止するため、装置の密閉化又は局所排気装置を設置すること。 適切な呼吸器保護具を着用すること。 | ||
| 保護具 | |||
| 呼吸用保護具 | 情報なし | ||
| 手の保護具 | 適切な保護手袋を着用すること。 | ||
| 眼の保護具 | 適切な眼の保護具を着用すること。 | ||
| 皮膚及び身体の保護具 | 適切な保護衣を着用すること。 | ||
| 9.物理的及び化学的性質 | |||
|---|---|---|---|
| 物理的状態 | |||
| 形状 | 固体 | ||
| 色 | 黄色 | ||
| 臭い | データなし | ||
| 臭いのしきい(閾)値 | 情報なし | ||
| pH | データなし | ||
| 融点・凝固点 | 270 ℃ : HSDB (2009) | ||
| 沸点、初留点及び沸騰範囲 | データなし | ||
| 引火点 | データなし | ||
| 蒸発速度(酢酸ブチル=1) | データなし | ||
| 燃焼性(固体、気体) | データなし | ||
| 燃焼又は爆発範囲 | データなし | ||
| 蒸気圧 | 4.82×10-20 mmHg (25 ℃ est ) : SRC (2009) | ||
| 蒸気密度 | データなし | ||
| 比重(相対密度) | データなし、(3.738 g/cm3 : HSDB (2009)) | ||
| 溶解度 | 水: 2.53 g/L (25 ℃) : HSDB (2009) もっとも一般的な溶剤に不溶。ジメチルホルムアミドに可溶 : Merck (14th, 2006) | ||
| n-オクタノール/水分配係数 | log Kow = -2.19 : HSDB (2009) | ||
| 自然発火温度 | データなし | ||
| 分解温度 | データなし | ||
| 粘度(粘性率) | データなし | ||
| 10.安定性及び反応性 | |||
|---|---|---|---|
| 反応性 | 「危険有害反応可能性」を参照。 | ||
| 化学的安定性 | 情報なし | ||
| 危険有害反応可能性 | 水溶液中でトランス型に徐々に変化する | ||
| 避けるべき条件 | データなし | ||
| 混触危険物質 | データなし | ||
| 危険有害な分解生成物 | データなし | ||
| 11.有害性情報 | |||
|---|---|---|---|
| 急性毒性 | |||
| 経口 | ラットLD50値は約20 mg/kg(EHC No.125(1991))であるとの報告に基づき、区分2とした。 | ||
| 経皮 | データなし。 | ||
| 吸入:ガス | GHSの定義における固体である。 | ||
| 吸入:蒸気 | データなし。 | ||
| 吸入:粉じん及びミスト | データなし。 | ||
| 皮膚腐食性及び皮膚刺激性 | ウサギを用いたパッチテスト(24時間適用)において、皮膚一次刺激指数0.13で軽度の刺激性(mild irritant)がみられる(EHC No.125(1991))ため、JIS分類基準の区分外(国連分類基準の区分3)とした。 | ||
| 眼に対する重篤な損傷性又は眼刺激性 | ウサギを用いた試験において、重度の刺激性(severely irritant)がみられる(EHC No.125(1991))ため、区分2Aとした。なお、水溶性の白金塩として「粉末は眼に対して灼熱感、流涙、結膜充血、時に羞明を引き起こし、角膜上皮に影響を与える可能性が示唆される。」(HSDB(2009))との記載がある。 | ||
| 呼吸器感作性 | 呼吸器感作性に関するデータはなく、分類できないとした。なお、EHC No.125(1991)において「本物質のような白金の中性錯体にアレルギー誘発性はない。これは、恐らく本物質が完全抗原を形成するタンパク質と反応しないためである。」との記載がある。 | ||
| 皮膚感作性 | EHC No.125(1991)において「本物質のような白金の中性錯体にアレルギー誘発性はない。これは、恐らく本物質が完全抗原を形成するタンパク質と反応しないためである。」との記載があり、区分外とした。 | ||
| 生殖細胞変異原性 | in vivo試験では、マウスの精母細胞を用いた染色体異常試験で陽性であり(PATTY(5th, 2001))、区分1Bとした。なお、その他in vivo試験では、マウスを用いた優性致死試験で陰性(IARC Suppl. No.7(1987))、マウスおよびラットの骨髄を用いた染色体異常試験で陽性(EHC No.125(1991)、PATTY(5th, 2001))、マウスの骨髄を用いた姉妹染色分体交換試験で陽性(EHC No.125(1991))、ラット体細胞DNAとの付加体形成試験で陽性(PATTY(5th, 2001))である。in vitro試験では、全てのエームス試験、染色体異常試験、小核試験で陽性である(EHC No.125(1991)、IARC vol.26(1981)、NTP DB(access on Oct. 2009))。 | ||
| 発がん性 | 【分類根拠】 (1)〜(3)のIARCの分類結果及び(4)〜(6)の試験結果に基づき、区分1Bとした。 IARCの分類見直しに伴い、旧分類を見直したが、他物質と併用された場合の分類であったため、本物質の分類は変更せず1Bのままとした。 (7)、(8)に示すようにエトポシドと本物質とブレオマイシンの併用療法は、ヒトに発がん性を示す。 【根拠データ】 (1)本物質単独での発がん性分類はIARCによりグループ2A(IARC Suppl. 7(1987))、NTPによりR(NTP RoC(14th, 2016))に分類されている。 (2)IARCは、1990年代のコホート調査報告の再評価結果である急性骨髄性白血病の増加に基づき、エトポシドと本物質とブレオマイシンの併用をグループ1に分類している(IARC 100A(2012))。 (3)誘発された急性骨髄性白血病にはエトポシドのようなトポイソメラーゼII 阻害剤によるものの顕著な特徴があったが、本物質はトポイソメラーゼII 阻害に関与しない。エトポシドは単独でもグループ1に分類されている(IARC 100A(2012))。 (4)マウスに複数回腹腔内投与した試験において、肺腺腫の発生増加がみられた(IARC Suppl. No.7(1987))。 (5)マウスの皮膚にプロモーターとしてクロトン油を塗布し腹腔内投与した試験において、皮膚乳頭腫の発生増加がみられた(IARC Suppl. No.7(1987))。 (6)ラットに複数回腹腔内投与した2つの試験において、白血病を誘発した(IARC Suppl. No.7(1987))。 【参考データ等】 (7)1990年代に実施されたエトポシドと本物質とブレオマイシンの併用療法に関する多数のコホート調査の再評価により、急性骨髄性白血病の増加が認められた(IARC 100A(2012))。 (8)本物質は、通常併用化学療法処方の主成分として、特にブレオマイシンやエトポシドとともに、精巣腫瘍の治療に用いられている(IARC 100A(2012))。 | ||
| 生殖毒性 | ヒトでは、本物質を含む抗がん剤の治療を妊娠初期に受けた13人の女性のうち、子供が生まれるまで妊娠を継続した5人中2人に新生児の低体重がみられ、自然流産が4人にみられた(PATTY(5th, 2001))との報告、本物質の治療開始後2ヶ月以内に無精子症が発症することが示された(HSDB(2009))との報告があり、医薬品添付文書において、「妊婦又は妊娠している可能性のある婦人には投与しないこと。(動物実験で、ラットにおいて催奇形作用、胎児致死率の増加、ウサギにおいて胎児致死率の増加が認められ、また、マウスにおいて催奇形作用、胎児致死作用が報告されている。)」、「授乳婦に投与する場合には、授乳を中止させること。(母乳中に移行することが報告されている。)」との記述があるため(ランダ注(シスプラチン製剤)添付文書(2009))、以上の結果より生殖毒性については区分1B、また授乳に対するまたは授乳を介した影響に関する追加区分とした。 | ||
| 特定標的臓器毒性(単回ばく露) | 本物質は抗がん剤として使用されており、ヒトのデータは、本物質を投与された患者における副作用を報告したものである。経口、経皮、吸入経路のデータは無く、単回か反復かの判断も困難であるが、急性影響として記載されている症状は、消化器への影響として難治性の吐気と嘔吐、骨髄の影響として白血球減少症、血小板減少症(IARC vol.26(1981))、腎臓への影響として尿細管の損傷、神経系への影響として聴力の低下、不明瞭な話し方、味覚障害、手の無感覚、歩行困難、深部腱反射の消失または減少、見当識障害、妄想症、感覚機能低下、運動機能低下がみられる(いずれもPIM 132(1992))ため、区分1(消化器、骨髄、腎臓、神経系)とした。なお、その他一時的で軽度の肝臓毒性がみられるが、肝臓への影響は稀である(PIM 132(1992))との記載があるため、分類には考慮しなかった。 | ||
| 特定標的臓器毒性(反復ばく露) | 本物質は抗がん剤として使用されており、ヒトのデータは、本物質を投与された患者における副作用を報告したものである。経口、経皮、吸入経路のデータは無いが、長期治療においてみられる症状は、骨髄への影響として骨髄抑制、貧血、血小板減少症、白血球減少症、腎臓への影響として糸球体ろ過率の著しい低下、神経系への影響として末梢神経障害、眼の神経炎、乳頭浮腫、足首の振動感覚と反射の減少、てんかん性発作、消化器への影響として強い吐気、嘔吐、胃腸疾患が記載されている(PATTY(5th, 2001)、PIM 132(1992))。よって、区分1(骨髄、腎臓、神経系、消化器系)とした。また、医薬品添付文書においては、重大な副作用として「急性腎不全、汎血球減少等の骨髄抑制、ショック、アナフィラキシー様症状、聴力低下・難聴、耳鳴、うっ血乳頭、球後視神経炎、皮質盲、脳梗塞、一過性脳虚血発作、溶血性尿毒症症候群、心筋梗塞、狭心症、うっ血性心不全、不整脈、溶血性貧血、間質性肺炎、抗利尿ホルモン不適合分泌症候群、劇症肝炎、肝機能障害、黄疸、消化管出血、消化性潰瘍、消化管穿孔、急性膵炎、高血糖、糖尿病の悪化、横紋筋融解症」(ランダ注(シスプラチン製剤)添付文書(2009))との記載があることから全身毒性とした。 | ||
| 吸引性呼吸器有害性 | データなし。 | ||
| 12.環境影響情報 | |||
|---|---|---|---|
| 生態毒性 | |||
| 水生環境有害性(急性) | データなし。 | ||
| 水生環境有害性(長期間) | データなし。 | ||
| オゾン層への有害性 | - | ||
| 13.廃棄上の注意 | |||
|---|---|---|---|
| 残余廃棄物 | 廃棄においては、関連法規ならびに地方自治体の基準に従うこと。 都道府県知事などの許可を受けた産業廃棄物処理業者、もしくは地方公共団体がその処理を行っている場合にはそこに委託して処理する。 廃棄物の処理を委託する場合、処理業者等に危険性、有害性を十分告知の上処理を委託する。 | ||
| 汚染容器及び包装 | 容器は洗浄してリサイクルするか、関連法規制ならびに地方自治体の基準に従って適切な処分を行う。 空容器を廃棄する場合は、内容物を完全に除去すること。 | ||
| 14.輸送上の注意 | ||||
|---|---|---|---|---|
| 該当の有無は製品によっても異なる場合がある。法規に則った試験の情報と、12項の環境影響情報とに基づいて、修正が必要な場合がある。 | ||||
| 国際規制 | ||||
| 国連番号 | 3249 | |||
| 国連品名 | MEDICINE, SOLID, TOXIC, N.O.S. | |||
| 国連危険有害性クラス | 6.1 | |||
| 副次危険 | 該当しない | |||
| 容器等級 | II | |||
| 海洋汚染物質 | 該当しない | |||
| MARPOL73/78附属書賖及び IBCコードによるばら積み 輸送される液体物質 | 該当しない | |||
| 国内規制 | ||||
| 海上規制情報 | 船舶安全法の規定に従う。 | |||
| 航空規制情報 | 航空法の規定に従う。 | |||
| 陸上規制情報 | 道路法の規定に従う。 | |||
| 特別な安全上の対策 | 道路法の規定によるイエローカード携行の対象物 | |||
| その他 (一般的) 注意 | 化学品を扱う場合の一般的な注意として、輸送に際しては、直射日光を避け、容器の破損、腐食、漏れのないように積み込み、荷崩れの防止を確実に行う。 重量物を上積みしない。 | |||
| 緊急時応急措置指針番号* | 151 | |||
| * 北米緊急時応急措置指針に基づく。米国運輸省が中心となって発行した「2008 Emergency Response Guidebook (ERG 2008)」(一般社団法人日本化学工業協会によって和訳されている(発行元:日本規格協会)に掲載されている。 | ||||
| 15.適用法令 | ||||
|---|---|---|---|---|
| 法規制情報は作成年月日時点に基づいて記載されております。事業場において記載するに当たっては、最新情報を確認してください。 | ||||
| 該当しない | ||||
| 16.その他の情報 | ||||
|---|---|---|---|---|
| 参考文献 | 各データ毎に記載した。 | |||
| [注意] 本SDSはJIS Z7253:2012 に準拠して作成しています。 | ||||