| 1.化学品及び会社情報 | |||
|---|---|---|---|
| 化学品の名称 | ベンゾフェノン | ||
| 化学品の英語名称 | Benzophenone | ||
| 製品コード | R03-B-010-MHLW | ||
| 供給者の会社名 | ○○○○株式会社 | ||
| 住所 | 東京都△△区△△町△丁目△△番地 | ||
| 電話番号 | 03-1234-5678 | ||
| ファックス番号 | 03-1234-5678 | ||
| 電子メールアドレス | 連絡先@検セ.or.jp | ||
| 緊急連絡電話番号 | 03-1234-5678 | ||
| 推奨用途及び使用上の制限 | 有機合成原料、医薬中間体、紫外線吸収剤、光重合開始剤 (NITE-CHRIPより引用) | ||
| 2.危険有害性の要約 | |||
|---|---|---|---|
| GHS分類 | |||
| 分類実施日 (物化危険性及び健康有害性) | R4.3.15、政府向けGHS分類ガイダンス(令和元年度改訂版(Ver2.0))を使用 | ||
| 物理化学的危険性 | - | ||
| 健康に対する有害性 | 急性毒性(経口) | 区分4 | |
| 発がん性 | 区分1B | ||
| 特定標的臓器毒性 (反復ばく露) | 区分2(肝臓、腎臓) | ||
| 分類実施日 (環境有害性) | ガイダンスVer.1.1 (GHS 4版, JIS Z7252:2014) | ||
| 環境に対する有害性 | 水生環境有害性 短期(急性) | 区分2 | |
| 水生環境有害性 長期(慢性) | 区分2 | ||
| GHSラベル要素 | |||
| 絵表示 |    | ||
| 注意喚起語 | 危険 | ||
| 危険有害性情報 | 飲み込むと有害 発がんのおそれ 長期にわたる、又は反復ばく露による肝臓、腎臓の障害のおそれ 長期継続的影響により水生生物に毒性 | ||
| 注意書き | |||
| 安全対策 | 使用前に取扱説明書を入手すること。 全ての安全注意を読み理解するまで取り扱わないこと。 粉じん/煙/ガス/ミスト/蒸気/スプレーを吸入しないこと。 取扱い後は手をよく洗うこと。 この製品を使用するときに、飲食又は喫煙をしないこと。 環境への放出を避けること。 保護手袋/保護衣/保護眼鏡/保護面を着用すること。 | ||
| 応急措置 | 飲み込んだ場合:気分が悪いときは医師に連絡すること。 ばく露又はばく露の懸念がある場合:医師の診察/手当てを受けること。 気分が悪いときは、医師の診察/手当てを受けること。 口をすすぐこと。 漏出物を回収すること。 | ||
| 保管 | 施錠して保管すること。 | ||
| 廃棄 | 内容物/容器を都道府県知事の許可を受けた専門の廃棄物処理業者に依頼して廃棄すること。 | ||
| 他の危険有害性 | 情報なし | ||
| 3.組成及び成分情報 | |||
|---|---|---|---|
| 化学物質・混合物の区別 | 化学物質 | ||
| 化学名又は一般名 | ベンゾフェノン | ||
| 慣用名又は別名 | 情報なし | ||
| 英語名 | Benzophenone Benzoylbenzene Diphenyl ketone Phenyl ketone | ||
| 濃度又は濃度範囲 | 情報なし | ||
| 分子式 (分子量) | C13H10O (182.22) | ||
| 化学特性 (示性式又は構造式) | 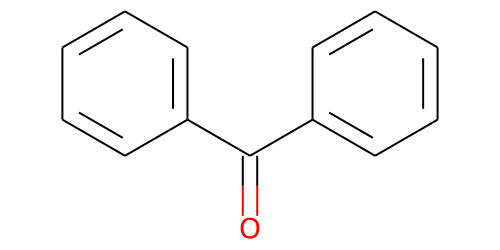 | ||
| CAS番号 | 119-61-9 | ||
| 官報公示整理番号(化審法) | 3-1258、4-125 | ||
| 官報公示整理番号(安衛法) | 情報なし | ||
| GHS分類に寄与する成分(不純物及び安定化添加物も含む) | 情報なし | ||
| 4.応急措置 | |||
|---|---|---|---|
| 吸入した場合 | 空気の新鮮な場所に移し、呼吸しやすい姿勢で休息させること。 | ||
| 皮膚に付着した場合 | 洗い流してから水と石鹸で皮膚を洗浄する。 | ||
| 眼に入った場合 | 水で数分間注意深く洗うこと。次にコンタクトレンズを着用していて容易に外せる場合は外すこと。 | ||
| 飲み込んだ場合 | 気分が悪いときは医師に連絡すること。 口をすすぐこと。 医師の診察/手当てを受けること。 気分が悪いときは、医師の診察/手当てを受けること。 漏出物を回収すること。 | ||
| 急性症状及び遅発性症状の最も重要な徴候症状 | 吸入 : 咽頭痛 皮膚 : 発赤 眼 : 発赤 | ||
| 応急措置をする者の保護に必要な注意事項 | 情報なし | ||
| 医師に対する特別な注意事項 | 情報なし | ||
| 5.火災時の措置 | |||
|---|---|---|---|
| 適切な消火剤 | 粉末消火薬剤、アルコール耐性泡消火薬剤、水噴霧、二酸化炭素 | ||
| 使ってはならない消火剤 | 棒状注水 | ||
| 火災時の特有の危険有害性 | 熱、火花及び火炎で発火するおそれがある。 激しく加熱すると燃焼する。 火災時に刺激性、腐食性及び毒性のガスを発生するおそれがある。 | ||
| 特有の消火方法 | 危険でなければ火災区域から容器を移動する。 安全に対処できるならば着火源を除去すること。 | ||
| 消火を行う者の特別な保護具及び予防措置 | 消火作業の際は、適切な自給式の呼吸器用保護具、防護服(耐熱性)を着用する。 | ||
| 6.漏出時の措置 | |||
|---|---|---|---|
| 人体に対する注意事項、保護具及び緊急措置 | 全ての着火源を取り除く。 直ちに、全ての方向に適切な距離を漏洩区域として隔離する。 関係者以外の立入りを禁止する。 密閉された場所に立入る前に換気する。 | ||
| 環境に対する注意事項 | 環境中に放出してはならない。 | ||
| 封じ込め及び浄化の方法及び機材 | 水で湿らせ、空気中のダストを減らし分散を防ぐ。 | ||
| 二次災害の防止策 | 情報なし | ||
| 7.取扱い及び保管上の注意 | |||
|---|---|---|---|
| 取扱い | |||
| 技術的対策 | 「8. ばく露防止及び保護措置」に記載の措置を行い、必要に応じて保護具を着用する。 | ||
| 安全取扱注意事項 | 使用前に取扱説明書を入手すること。 全ての安全注意を読み理解するまで取り扱わないこと。 粉じん/煙/ガス/ミスト/蒸気/スプレーを吸入しないこと。 | ||
| 接触回避 | 「10. 安全性及び反応性」を参照。 | ||
| 衛生対策 | 取扱い後は手をよく洗うこと。 この製品を使用するときに、飲食又は喫煙をしないこと。 | ||
| 保管 | |||
| 安全な保管条件 | 施錠して保管すること。 | ||
| 安全な容器包装材料 | 国連危険物輸送勧告モデル規則で規定されている容器を使用する。 | ||
| 8.ばく露防止及び保護措置 | ||||
|---|---|---|---|---|
| 許容濃度等については日本産衛学会の「許容濃度の勧告」及びACGHIの「TLVs and BEIs」について記載しています。 | ||||
| 管理濃度 | 未設定 | |||
| 許容濃度等 | ||||
| 日本産衛学会(2021年版) | 第3種粉じん: その他の無機及び有機粉じん* 吸入性粉じん: 2 mg/m3 総粉じん: 8 mg/m3 * 多量の粉じんの吸入によるじん肺を予防する観点から、この値以下とすることが望ましいとされる濃度。 | |||
| ACGIH(2022年版) | PNOS* TLV: 3 mg/m3 (Respirable particles) PNOS* TLV: 10 mg/m3 (Inhalable particles) * Particles (insoluble or poorly soluble) Not Otherwise Specified | |||
| 設備対策 | 取り扱いの場所の近くに、洗眼及び身体洗浄のための設備を設ける。 作業場では全体換気を行う。 設備は可能であれば密閉系とし局所排気装置を用いる。 粉じんが発生する場合は防爆型電気設備および照明を用いる。 | |||
| 保護具 | ||||
| 呼吸用保護具 | 作業者が粉塵に暴露される場合は呼吸保護具(防じんマスク等)の着用を検討する。 防じんマスクの選択については、以下の点に留意する。 -酸素濃度が18%未満の場所では使用しない。また、有害なガスが存在する場所においては防じんマスクを使用せず、その他の呼吸用保護具の利用を検討すること。 -防じんマスクは、日本工業規格(JIS T8151)に適合した、作業に適した性能及び構造のものを選ぶ。その際、取扱説明書等に記載されているデータを参考にする。 | |||
| 手の保護具 | 保護手袋を着用する。 | |||
| 眼の保護具 | 保護眼鏡を着用する。 | |||
| 皮膚及び身体の保護具 | 保護衣を着用する。 | |||
| 9.物理的及び化学的性質 | |||
|---|---|---|---|
| 物理的状態 | |||
| 物理状態 | 固体 (20℃、1気圧) (GHS判定) | ||
| 色 | 白色 | ||
| 臭い | 花香気 | ||
| 融点/凝固点 | 48.5 ℃(ICSC(2010)) 49 ℃(GESTIS(2021)) 47 ℃(PubChem(2021)) | ||
| 沸点、初留点及び沸騰範囲 | 305 ℃(GESTIS(2021)、ICSC(2010)) 305.9 ℃(PubChem(2021)) | ||
| 可燃性 | 可燃性(ICSC(2010)) | ||
| 爆発下限界及び爆発上限界/可燃限界 | データなし | ||
| 引火点 | 138~155 ℃(GESTIS(2021)) 270 ℃(PubChem(2021)) ?110 ℃(Lange(2017)) | ||
| 自然発火点 | 560 ℃(GESTIS(2021)) | ||
| 分解温度 | ?320 ℃(GESTIS(2021)、ICSC(2010)) | ||
| pH | データなし | ||
| 動粘性率 | データなし | ||
| 溶解度 | 水: 0.14 g/L(GESTIS(2021)) 水に不溶(ICSC(2010)) アルコール、エーテル、クロロホルムに可溶(Lewis(2001)) | ||
| n-オクタノール/水分配係数 | Log Kow: 3.38(ICSC(2010)) Log Kow: 3.18(PubChem(2021)) | ||
| 蒸気圧 | 1.93X10-3 mm Hg(25℃)(PubChem(2021)) 0.00 mm Hg(PubChem(2021)) | ||
| 密度及び/又は相対密度 | 1.09 g/cm3(50℃)(GESTIS(2021)) 1.118 (18℃)(Merck(2013)) 1.085 (122°F)(PubChem(2021)) | ||
| 相対ガス密度 | 6.3 (空気=1)(ICSC(2010)) | ||
| 粒子特性 | データなし | ||
| 10.安定性及び反応性 | |||
|---|---|---|---|
| 反応性 | 「危険有害反応可能性」を参照。 | ||
| 化学的安定性 | 法規制に従った保管及び取扱においては安定と考えられる。 | ||
| 危険有害反応可能性 | >320℃で分解する。可燃性。燃焼すると、有毒なガスを生成する。強酸化剤と反応する。火災や爆発の危険を生じる。 | ||
| 避けるべき条件 | 熱 | ||
| 混触危険物質 | 強酸化剤 | ||
| 危険有害な分解生成物 | 情報なし | ||
| 11.有害性情報 | ||||
|---|---|---|---|---|
| 急性毒性 | ||||
| 経口 | 【分類根拠】 (1)~(4)より、有害性の高い区分を採用し、区分4とした。 【根拠データ】 (1)ラットのLD50:1,900 mg/kg(MOE初期評価 (2019)、NTP TR533 (2006)) (2)ラットのLD50:> 10,000 mg/kg(MOE初期評価 (2019)、AICIS IMAP (2015)、NTP TR533 (2006)) | |||
| 経皮 | 【分類根拠】 (1)、(2)より、区分に該当しない。 【根拠データ】 (1)ウサギのLD50:3,535 mg/kg(MOE初期評価 (2019)、NTP TR533 (2006)) (2)ウサギのLD50:> 2,000 mg/kg(AICIS IMAP (2015)) | |||
| 吸入: ガス | 【分類根拠】 GHSの定義における固体であり、区分に該当しない。 | |||
| 吸入: 蒸気 | 【分類根拠】 データ不足のため分類できない。 | |||
| 吸入: 粉じん及びミスト | 【分類根拠】 データ不足のため分類できない。 | |||
| 皮膚腐食性及び皮膚刺激性 | 【分類根拠】 (1)より、区分に該当しない。なお、新たな知見に基づき、分類結果を変更した。 【根拠データ】 (1)ウサギ(n=4)を用いた皮膚刺激性試験(OECD TG 404、GLP、2~100%(原液)、半閉塞、4時間適用、72時間観察)において、濃度100%まで皮膚刺激性の徴候は認められなかったとの報告がある(AICIS IMAP (2015)、REACH登録情報 (Accessed Dec. 2021))。 | |||
| 眼に対する重篤な損傷性又は眼刺激性 | 【分類根拠】 (1)~(3)より、区分に該当しない。なお、新たな知見に基づき、分類結果を変更した。 【根拠データ】 (1)ウサギ(n=3)を用いた眼刺激性試験において、適用1時間後に結膜及び瞬膜に軽微~中等度の紅斑がみられ、24時間後まで持続した。48時間後に軽微な紅斑が1匹にみられただけで、14日までに全て正常に回復したとの報告がある(Patty (6th, 2012))。 (2)ウサギ(n=6)を用いた眼刺激性試験において、軽微な反応しか生じなかったとの報告がある(REACH登録情報 (Accessed Dec. 2021)、AICIS IMAP (2015))。 (3)ウサギを用いた眼刺激性試験において、眼刺激性はみられなかったとの報告がある(REACH登録情報 (Accessed Dec. 2021))。 | |||
| 呼吸器感作性 | 【分類根拠】 データ不足のため分類できない。 | |||
| 皮膚感作性 | 【分類根拠】 (1)、(2)より、区分に該当しない。 【根拠データ】 (1)本物質の6%溶液を用いてボランティア 25 人で実施した感作性試験では、陽性反応はみられなかった(MOE 初期評価 (2019)、REACH登録情報 (Accessed Dec. 2021))。 (2)モルモット(n=20)を用いたMaximisation試験(皮内投与:1%溶液)において、全例で陽性反応はみられなかった(AICIS IMAP (2015)、REACH登録情報 (Accessed Dec. 2021))。 【参考データ等】 (3)モルモット(n=10)を用いた修正Draize法による皮膚感作性試験(皮内投与:1%溶液を4回適用)において、感作性反応はみられなかったとの報告がある(AICIS IMAP (2015)、REACH登録情報 (Accessed Dec. 2021))。 | |||
| 生殖細胞変異原性 | 【分類根拠】 (1)、(2)より区分に該当しない。なお、ガイダンスに基づき分類結果を変更した。 【根拠データ】 (1)In vivoでは、3系統のマウスの骨髄細胞を用いた4つの小核試験(単回腹腔内投与(500~2,000 mg/kg、又は100~600 mg/kg)、3日間腹腔内投与(200~500 mg/kg)、14週間混餌投与(1,250~20,000 ppm(200~4,200 mg/kg/day))の結果はいずれも陰性であった(AICIS IMAP (2015)、EFSA (2017)、Government of Canada, Screening Assessment (2021))。 (2)In vitroでは、細菌復帰突然変異試験、マウスリンパ腫L5178Y細胞を用いた遺伝子突然変異試験で陰性であった(AICIS IMAP (2015)、EFSA (2017)、Government of Canada, Screening Assessment (2021))。 【参考データ等】 (3)本物質は利用可能な試験結果から、遺伝毒性を有さないと考えられ、本物質の発がん性の作用機序に遺伝毒性は関連しないとみられている(EFSA (2017)、CLH Report (2019)、ECHA RAC Opinion (2020))。 | |||
| 発がん性 | 【分類根拠】 (1)、(2)より、動物種2種で悪性を含む腫瘍の発生増加が認められ、動物実験において発がん性の十分な証拠があると考えられることから、区分1Bとした。なお、新たな評価に基づき分類結果を変更した。 【根拠データ】 (1)ラットを用いた2年間混餌投与(312~1,250 ppm)による発がん性試験において、雄に腎尿細管腺腫(高用量群)及び単核球白血病の発生頻度(低及び中用量群)、雌に単核球白血病の発生頻度(中用量群)が認められた(IARC 101 (2013))。さらに、EFSAをはじめEUの評価では雌に組織球性肉腫の増加(稀少がん))が追加された(NTP TR533(2006)、EFSA (2017)、CLH Report (2019)、ECHA RAC Opinion (2019)、MOE初期評価 (2019)、Government of Canada, Screening Assessment (2021))。 (2)マウスを用いた2年間混餌投与(312~1,250 ppm)による発がん性試験において、雄に肝細胞腺腫単独、及び肝細胞腺腫と肝細胞がんの合計発生頻度、雌に組織球性肉腫(稀少がん)の増加が認められた(IARC 101 (2013))。さらに、EFSAをはじめEUの評価では雄に肝芽腫の増加(稀少がん)も追加された(NTP TR533(2006)、EFSA (2017)、CLH Report (2019)、ECHA RAC Opinion (2019)、MOE初期評価 (2019)、Government of Canada, Screening Assessment (2021))。 (3)(1)、(2)より、雌マウスと雌ラットにおける稀少がんの組織球性肉腫の発生頻度の増加も含め、2動物種で発がん性の証拠が得られた。ECHA RACは、低頻度の発生率であるが、組織球性肉腫は本物質のばく露に関連したもので、生物学的にも重要である。また、雄マウスには稀少がんの肝芽腫の発生もみられており、Category 2からCategory 1Bに引き上げるのが妥当であると結論した(ECHA RAC Opinion (2019))。 (4)国内外の評価機関による既存分類結果として、IARCでグループ2Bに(IARC 101 (2013))、日本産業衛生学会で第2群Bに分類されている(産衛学会許容濃度等の勧告 (2020))。 【参考データ等】 (5)雌マウスを用いた120週間経皮投与(5~50%、2回/週)による発がん性試験では、適用部位を含め、腫瘍の発生増加は認められなかった(IARC101 (2013)、EFSA (2009)、EU REACH CoRAP (2018)、CLH Report (2019)、MOE初期評価 (2019)、Government of Canada (2021))。 | |||
| 生殖毒性 | 【分類根拠】 (1)~(3)より区分に該当しない。なお、(1)より、母動物の一般毒性用量で流産/早産の発生頻度の増加がみられ、妊娠早期中断を示唆する所見がみられているが、母体毒性に起因するものと考えられる。 【参考データ等】 (1)雌ウサギを用いた強制経口投与による発生毒性試験(妊娠6~29日、5~45 mg/kg/day)において、母動物毒性(死亡(2/24)、体重増加抑制、摂餌量減少)がみられる中用量(25 mg/kg/day)以上で妊娠の早期中断(流産又は早産)の発生率増加(対照群、低・中・高用量群で各々0/24、0/24、3/22(4.5%)、7/19(36.8%))がみられた。胎児には高用量群で体重の低値がみられたのみであったとの報告がある(EFSA (2009; 2017)、AICIS IMAP (2015)、Government of Canada, Screening Assessment (2021)、NTP (2004))。 (2)ラットを用いた混餌投与による2世代生殖毒性試験(OECD TG416、100~2,000 ppm)において、F0及びF1親動物には100 ppm(6.5 mg/kg/day(雄)、8.4 mg/kg/day(雌))以上で肝臓影響(重量増加、肝細胞肥大:適応性変化)、450 ppm(29 mg/kg/day(雄)、38 mg/kg/day(雌))以上では体重増加抑制、摂餌量減少及び腎臓影響(重量増加、近位尿細管拡張、近位尿細管上皮再生)がみられたが、生殖能への影響は認められなかった。F1及びF2児動物には2,000 ppm(130 mg/kg/day(雄)、167 mg/kg/day(雌))で体重増加抑制がみられただけであったとの報告がある(EFSA (2009; 2017)、AICIS IMAP (2015)、Government of Canada, Screening Assessment (2021))。 (3)雌ラットを用いた強制経口投与による発生毒性試験(妊娠6~19日、100~300 mg/kg/day)において、母動物毒性(体重低下、症状(嗜眠、立毛)、肝臓・腎臓重量増加)がみられる低用量から骨化遅延(胸骨分節の未骨化)、中用量から骨格変異(過剰肋骨)、高用量では腹当たりの胎児体重の低値がみられたとの報告がある(EFSA (2009; 2017)、AICIS IMAP (2015)、MOE初期評価 (2019)、Government of Canada, Screening Assessment (2021))。 | |||
| 特定標的臓器毒性 (単回ばく露) | 【分類根拠】 データ不足のため分類できない。なお、(1)は致死量付近でみられた影響であることから、根拠データとして採用していない。 【参考データ等】 (1)マウスを用いた単回経口投与試験において、致死量で鎮静、進行性の自発運動抑制、不安定歩行、振戦及び呼吸器障害がみられたとの報告がある。なお、LD50は2,895 mg/kgであった(REACH登録情報 (Accessed Dec. 2021))。 | |||
| 特定標的臓器毒性 (反復ばく露) | 【分類根拠】 (1)~(4)より、区分2(肝臓、腎臓)とした。なお、(1)より、血液系への影響がみられたが、(3)において、同種の動物を用いたより長期の試験では区分に該当する範囲でみられなかったため、標的臓器として採用していない。ガイダンスに基づき、分類結果を変更した。 【根拠データ】 (1)ラットを用いた混餌投与による28日間反復経口投与試験において、100 mg/kg/day(90日換算:31.1 mg/kg/day、区分2の範囲)で体重増加抑制、血清アルブミンの高値、肝臓の絶対及び相対重量、腎臓の相対重量の高値、肝細胞肥大、尿素窒素の高値(雄)、赤血球数の減少(雌)、ヘマトクリットの低値(雌)、総ビリルビン(雌)、総タンパクの高値(雌)がみられたとの報告がある(MOE初期評価 (2019)、Government of Canada (2021))。 (2)ラットを用いた混餌投与による14週間反復経口投与試験(OECD TG408)において、75 mg/kg/day(区分2の範囲)で体重の低値(雌)、肝臓影響(重量増加、小葉中心性肝細胞肥大、細胞質空胞化、肝ミクロソームのチトクロムP450 2Bの誘導(雌))、腎臓影響(重量増加、尿細管上皮の再生)がみられたとの報告がある(AICIS IMAP (2015)、MOE初期評価 (2019)、EFSA (2009, 2017)、EU REACH CoRAP (2018))。 (3)ラットを用いた混餌投与による105週間経口投与試験において、312 ppm(15.6 mg/kg/day、区分2の範囲)で小葉中心性肝細胞肥大、尿細管過形成、甲状腺C細胞過形成、腎盂移行上皮過形成(雄)、腎症増悪(雄)、慢性活動性肝炎・胆管過形成(雌)が、625 ppm(31.3 mg/kg/day、区分2の範囲)で慢性活動性肝炎(雄)、肝臓の嚢胞変性(雄)、副甲状腺の過形成(雄)、腺胃の石灰化(雄)、体重の低値(雌)、腎症増悪(雌)がみられたとの報告がある(MOE初期評価 (2019)、AICIS IMAP(2019)、EFSA (2009; 2017)、EU REACH CoRAP (2018))。 (4)マウスを用いた混餌投与による105週間経口投与試験において、312 ppm(15.6 mg/kg/day、区分2の範囲)で小葉中心性肝細胞肥大、肝細胞の多核化(雄)、肝臓の慢性活動性炎症(雄)、腎症の増悪(雄)、脾臓リンパ濾胞の過形成(雄)、体重増抑制(雌)、腎症(雌)、腎臓の石灰化(雌)、脾臓リンパ濾胞の過形成(雌)、造血細胞の増殖(雌)が、625 ppm(31.3 mg/kg/day、区分2の範囲)で肝細胞の壊死(雄)、肝臓の嚢胞変性(雄)、腎皮質の嚢胞(雄)が、1,250 ppm(62.5 mg/kg/day、区分2の範囲)で嗅上皮における呼吸上皮化生、明細胞性変異肝細胞巣(雄)、精巣の石灰化(雄)、腎症の増悪(雌)がみられたとの報告がある(MOE初期評価 (2019)、AICIS IMAP(2019)、EFSA (2009; 2017)、EU REACH CoRAP (2018))。 | |||
| 誤えん有害性* | 【分類根拠】 データ不足のため分類できない。 | |||
| * JIS Z7252の改訂により吸引性呼吸器有害性から項目名が変更となった。 | ||||
| 12.環境影響情報 | |||
|---|---|---|---|
| 生態毒性 | |||
| 水生環境有害性 短期(急性) | 藻類(Pseudokirchneriella subcapitata)72時間ErC50 =3.53 mg/L(環境庁生態影響試験, 1998、環境省リスク評価第6巻, 2008)であることから、区分2とした。 | ||
| 水生環境有害性 長期(慢性) | 慢性毒性データを用いた場合、急速分解性がなく(難分解性、BODによる分解度:0%(既存点検, 1980))、甲殻類(オオミジンコ)の21日間NOEC = 0.2 mg/L(環境庁生態影響試験, 1998、環境省リスク評価第6巻, 2008)であることから、区分2となる。 慢性毒性データが得られていない栄養段階に対して急性毒性データを用いた場合、急速分解性がなく(難分解性、BODによる分解度:0%(既存点検, 1980))、魚類(ファットヘッドミノー)96時間LC50 = 10.9 mg/L(環境省リスク評価第6巻, 2008)であることから、区分3となる。 以上の結果から、区分2とした。 | ||
| 残留性・分解性 | 化審法分解度試験:難分解性(化学物質安全性点検結果等(分解性・蓄積性)) | ||
| 生態蓄積性 | 化審法濃縮度試験:低濃縮性(化学物質安全性点検結果等(分解性・蓄積性)) | ||
| 土壌中の移動性 | 情報なし | ||
| オゾン層への有害性 | 当該物質はモントリオール議定書の附属書に列記されていない。 | ||
| 13.廃棄上の注意 | |||
|---|---|---|---|
| 化学品(残余廃棄物)、当該化学品が付着している汚染容器及び包装の安全で、かつ、環境上望ましい廃棄、又はリサイクルに関する情報 | 廃棄においては、関連法規ならびに地方自治体の基準に従うこと。 都道府県知事などの許可を受けた産業廃棄物処理業者、もしくは地方公共団体がその処理を行っている場合にはそこに委託して処理する。 廃棄物の処理を委託する場合、処理業者等に危険性、有害性を十分告知の上処理を委託する。 | ||
| 容器は洗浄してリサイクルするか、関連法規制並びに地方自治体の基準に従って適切な処分を行う。 空容器を廃棄する場合は、内容物を完全に除去すること。 | |||
| 14.輸送上の注意 | ||||
|---|---|---|---|---|
| 本物質のGHS分類結果に基づく国際規制の分類等は、以下の通りと推定されるが、該否は製品によって異なる場合がある。輸送危険物の分類は、容器等級を含め、荷送人が責任をもって判断することとされているため、輸送の際には、個々の貨物について、製品の状態、形状等も考慮し、輸送モード (航空、船舶) を規制する法規に沿って事業者が判断する必要がある。 | ||||
| 国際規制 | ||||
| 国連番号 | 3077 | |||
| 品名(国連輸送名) | 環境有害性物質(固体)、n.o.s. | |||
| 国連分類 | 9 | |||
| 副次危険 | - | |||
| 容器等級 | Ⅲ | |||
| 海洋汚染物質 | 該当する | |||
| MARPOL73/78附属書Ⅱ及びIBCコードによるばら積み輸送される液体物質 | 該当しない | |||
| 国内規制 | ||||
| 海上規制情報 | 船舶安全法の規定に従う。 | |||
| 航空規制情報 | 航空法の規定に従う。 | |||
| 陸上規制情報 | 該当しない | |||
| 特別な安全上の対策 | 該当しない | |||
| その他 (一般的) 注意 | 輸送に際しては、直射日光を避け、容器の破損、腐食、漏れのないように積み込み、荷崩れの防止を確実に行う。 重量物を上積みしない。 | |||
| 緊急時応急措置指針番号* | 171 | |||
| * 北米緊急時応急措置指針に基づく。米国運輸省が中心となって発行した「2020 Emengency Response Guidebook (ERG 2020)」(一般社団法人日本化学工業協会によって和訳されている(発行元:日本規格協会)に掲載されている。 | ||||
| 15.適用法令 | ||||
|---|---|---|---|---|
| 法規制情報は作成年月日時点に基づいて記載されております。事業場において記載するに当たっては、最新情報を確認してください。 | ||||
| 労働安全衛生法 | 該当しない | |||
| 化学物質排出把握管理促進法(PRTR法) | 第一種指定化学物質(法第2条第2項、施行令第1条別表第1) | |||
| 毒物及び劇物取締法 | 該当しない | |||
| 船舶安全法 | 有害性物質(危規則第3条危険物告示別表第1) | |||
| 航空法 | その他の有害物件 | |||
| 16.その他の情報 | ||||
|---|---|---|---|---|
| 参考文献 | ||||
| 9項、11項については各データ毎に記載。その他の各項については以下を参照。 ・NITE化学物質総合情報提供システム(NITE-CHRIP) ・International Chemical Safety Cards (ICSC) ・Hazardous Substances Data Bank (HSDB) ・GESTIS Substance database (GESTIS) ・ERG 2020版 緊急時応急措置指針-容器イエローカードへの適用 ・一般社団法人日本化学工業協会 編「GHS対応ガイドライン ラベル及び表示・安全デ-タシ-ト作成指針」 | ||||